Внимание! Статья адресована врачам-специалистам
DOI: https://doi.org/ 10.24412/2076-4812-2026-3378-83-86
Yusupalikhodjaeva S.Kh.1, Shomurodova G.Kh.1, Radjabov O.I.2, Vypova N.L.2
1Tashkent State Medical University, Uzbekistan
2A.S. Sadykov Institute of Bioorganic Chemistry, Academy of Sciences of the Republic of Uzbekistan, Tashkent
Histomorphological evaluation of tissue reaction
and biodegradation of collagen composites in subcutaneous implantation in rodents
Резюме. Эндопародонтальные поражения являются патогенетическим комплексом воспаления, вовлекающим поражения эндодонта и деструкцию пародонта. Проведено исследование гистоморфологических изменений биодеградации коллаген-гидроксиапатитового и коллаген-гиалуронового композитов при подкожной имплантации у 24 белых нелинейных крыс (n=6 в группах). На 3-й неделе при применении коллаген-гиалуронового композитов отмечена полноценная резорбция с минимальной геморрагией и сохранной дермальной архитектурой. В группе, где применялся коллаген-гидроксиапатитовый композит, на 4-й неделе отмечена деградация с проявлением фиброзного воспаления, васкуляризацией грануляций, коллагеногенезом и дистрофической кальцификацией (p<0,05).
Ключевые слова: эндопародонтальные поражения, композит «коллаген – гидроксиапатит», композит «коллаген – гиалуроновая кислота».
Для цитирования: Юсупалиходжаева С.Х., Шомуродова Г.Х., Раджабов О.И., Выпова Н.Л. Гистоморфологическая оценка тканевой реакции и биодеградации коллагеновых композитов при подкожной имплантации // Медицинские новости. – 2026. – №3. – С. 83–86.
Summary. Endo-periodontal lesions represent a pathogenetic complex of inflammation involving endodontic damage and periodontal destruction.A study of histomorphological changes in the biodegradation of collagen-hydroxyapatite and collagen-hyaluronic composites was conducted via subcutaneous implantation in 24 white nonlinear rats (n=6 per group). By week 3 with collagen-hyaluronic application, complete resorption was noted with minimal hemorrhage and preserved dermal architecture. In the collagen-hydroxyapatite group by week 4, degradation was observed with fibrotic inflammation, granulation vascularization, collagenogenesis, and dystrophic calcification (p<0.05).
Keywords: endo-periodontal lesions, collagen-hydroxyapatite composite, collagen-hyaluronic acid composite.
For citation: Yusupalikhodjaeva S.Kh., Shomurodova G.Kh., Radjabov O.I., Vypova N.L. Histomorphological evaluation of tissue reaction and biodegradation of collagen composites in subcutaneous implantation in rodents // Meditsinskie novosti. – 2026. – N3. – P. 83–86.
Эндопериодонтальные поражения (ЭПП) представляют собой клинически сложную форму патологии зуба, сочетающую инфекционно-воспалительный процесс в эндодонтии с распространением воспаления на пародонтальные ткани, альвеолярный гребень и периапикальную область до уровня сообщения между корневым каналом и пародонтальным карманом [3, 6, 8].
У лиц с умеренным и тяжелым хроническим пародонтитом и неадекватно пролеченной эндодонтической патологией наличие фистuлюзных трактов, глубоких пародонтальных карманов и комбинированных периапикальных поражений способствует развитию ЭПП [4, 5, 13].
ЭПП проявляются следующими характерными клиническими признаками: прогрессирующая резорбция альвеолярной кости, атрофия десны, повышение гиперестезии к термическим и механическим раздражителям, персистирующая ноющая боль, которая обусловливает значительный риск удаления зуба при его сохранности коронковой и корневой части. При ЭПП отмечается взаимосвязь между системой корневых каналов и пародонтальным карманом, обеспечивающая непрерывное двунаправленное распространение патогенных микроорганизмов и воспалительных медиаторов между эндодонтальными и пародонтальными тканями, что усугубляет прогрессирование заболевания [4, 8]. ЭПП на рентгенограммах проявляются с периапикальными зонами остеолиза и пародонтальными карманами глубиной свыше 6 мм, проявляющимися вертикальными и горизонтальными костными дефектами вдоль корня, что затрудняет дифференциацию с изолированными эндодонтическими или пародонтальными процессами. С развитием методов диагностики в стоматологии (КЛКТ, трехмерная томография и рентгенография высокого разрешения), а также усовершенствованием диагностики распространенности хронического пародонтита значительно улучшилась частота выявления ЭПП у пациентов с комбинированной пародонтальной и эндодонтической патологией [6, 7]. Морфологическая сложность диагностики ЭПП способствует частой встречаемости комбинированных горизонтальных и вертикальных дефектов кости и межкорневых резорбций, ограничивающих эффективность традиционных методов лечения и подчеркивающих необходимость разработки биоактивных остеопластических и регенеративных биоматериалов, которые содержат композиты на основе коллагена и гидроксиапатита [8, 11].
Современные исследования подтверждают, применение коллаген-гидроксиапатитовых композитов содействует устранению объемных дефектов кости, являясь реставраторами дефектов, но и биосовместимыми остеокондуктивными основами, обеспечивающими тканевую интеграцию и стабилизацию костной регенерации при эндопародонтальных поражениях. По результатам исследований, материалы на основе коллагена с гидроксиапатитом усиливают остеогенез и повышают выживаемость зубов, а их комбинация с тромбоцитарной плазмой дополнительно ускоряет репаративные процессы, что доказывают клинические наблюдения [1, 9–11].
Кроме того, накопленные данные свидетельствуют о том, что мембраны и костные субстанты на основе коллаген-гидроксиапатита могут служить носителями антимикробных агентов и способствовать локальной минерализации в эндодонтальных и пародонтальных поражениях [9–12].
Таким образом, использование регенеративных коллаген-гидроксиапатитовых материалов для патогенетически обоснованной терапии ЭПП оптимизирует комплексные протоколы локального лечения, подчеркивая важность клинико-морфологического анализа для контроля эффективности.
Цель исследования – оценить характеристику резорбции и гистоморфологического ответа тканей на коллаген-гидроксиапатитовые и коллаген-гиалуроновые композиты в модели подкожной имплантации у грызунов.
Материалы и методы
Эксперимент был выполнен на 24 белых нелинейных крысах обоих полов массой тела 250±25 г. Животных случайным образом распределили по двум экспериментальным группам (по 6 – в группе). Все крысы содержались в стандартных условиях вивария с естественным световым режимом, свободным доступом к пище и воде, а также контролируемыми параметрами окружающей среды (температура 22–24 °C и относительная влажность 40–60%).
Все экспериментальные процедуры с животными проводились в соответствии с Европейской конвенцией о защите позвоночных животных, используемых для экспериментальных и иных научных целей, и были одобрены локальным этическим комитетом (Протокол №4 от 9 сентября 2024 г.).
В первую экспериментальную группу имплантировали образцы композита «коллаген – гидроксиапатит» (диски размером 5×5 мм массой 10 мг), во вторую группу – композиты «коллаген – гиалуроновая кислота» аналогичных размеров и массы. Исследуемые биоматериалы были получены в виде лиофилизированных белых пластин размером 72×72 мм и толщиной 3–5 мм. Перед имплантацией из пластин асептически вырезали стерильные фрагменты размером 10×10×2 мм. Подкожная имплантация проводилась в межлопаточной области под общей анестезией, вызванной внутрибрюшинным введением тиамина натрия в дозе 50 мг/кг. Хирургическую рану ушивали послойно узловыми швами нерассасывающимся шовным материалом.
Животных выключали из эксперимента на 2-й, 4-й и 6-й неделях после имплантации (по 2 животных в группе на каждом этапе) путем передозировки анестетика в соответствии с руководством ISO 10993-2. Имплантат вместе с окружающими тканями и регионарными лимфатическими узлами эксцидировали для последующей морфологической оценки.
Макроскопический анализ кожи и фиброзной капсулы изучен по цвету, на наличие гематом, по массе, с последующим их гистологическим анализом. Образцы для гистологического исследования фиксировали 48 часов в 10% нейтральном буферном формалине, промывали, проводили обезвоживание в градиенте этанолов в восходящем порядке от 70–100%, затем заливали в парафин по стандартному гистологическому протоколу. Полученные срезы толщиной 5–7 мкм окрашивали гематоксилином и эозином. Гистологическое исследование проводили с помощью бинокулярного светового микроскопа при увеличениях ×40 и ×100. Микрофотографии получали с помощью цифровой камеры HM-35 в нативном разрешении.
Результаты
При изучении массы животных в первой экспериментальной группе (коллаген – гидроксиапатит) определилось увеличение массы в 1,31 раза к 4-й неделе и в 1,48 раза к 6-й неделе относительно исходного уровня на 2-й неделе (193,0±16,8 г). Масса лимфоузлов выросла незначительно – в 1,004 раза на 4-й неделе и в 1,11 раза – на 6-й неделе по сравнению с таковой на 2-й неделе (50,2±4,6 мг). В первой экспериментальной группе масса капсулы и кожи на 2-й неделе составила 21,6±1,8 мг с сохранением точечных гематом во всех периодах наблюдения.Динамика макроскопических изменений периимплантационных капсул представлена в таблице 1. Масса капсулы в группе коллаген – гидроксиапатит была значительно выше в ранние сроки (p<0,05). Полная резорбция композита «коллаген – гиалуроновая кислота» произошла к 3-й неделе, тогда как композит «коллаген – гидроксиапатит» полностью рассосался к 4-й неделе после имплантации.
В 1 группе (композит «коллаген – гидроксиапатит») на всем протяжении исследования наблюдали выраженный фиброзно-репаративный тканевой ответ. На 2-й неделе зона имплантации была окружена зрелой грануляционной тканью с многочисленными сосудами тонкой стенки, периваскулярным оте-ком и инфильтрацией макрофагами и фибробластами; коллагеновые волокна по периферии были слабо организованы (табл. 1). К 4-й неделе интенсифицированный коллагеногенез привел к формированию толстых грубых коллагеновых пучков с уменьшенной васкуляризацией и минимальной клеточной инфильтрацией, при этом сохранялись остаточные фрагменты имплантата. К 6-й неделе ремоделирование привело к формированию зрелой грубой фиброзной рубцовой ткани с дистрофической кальцификацией, деструкцией кожных придатков и выраженным снижением сосудистости, что свидетельствует о фибротическом заживлении (см. табл. 1).
.jpg)
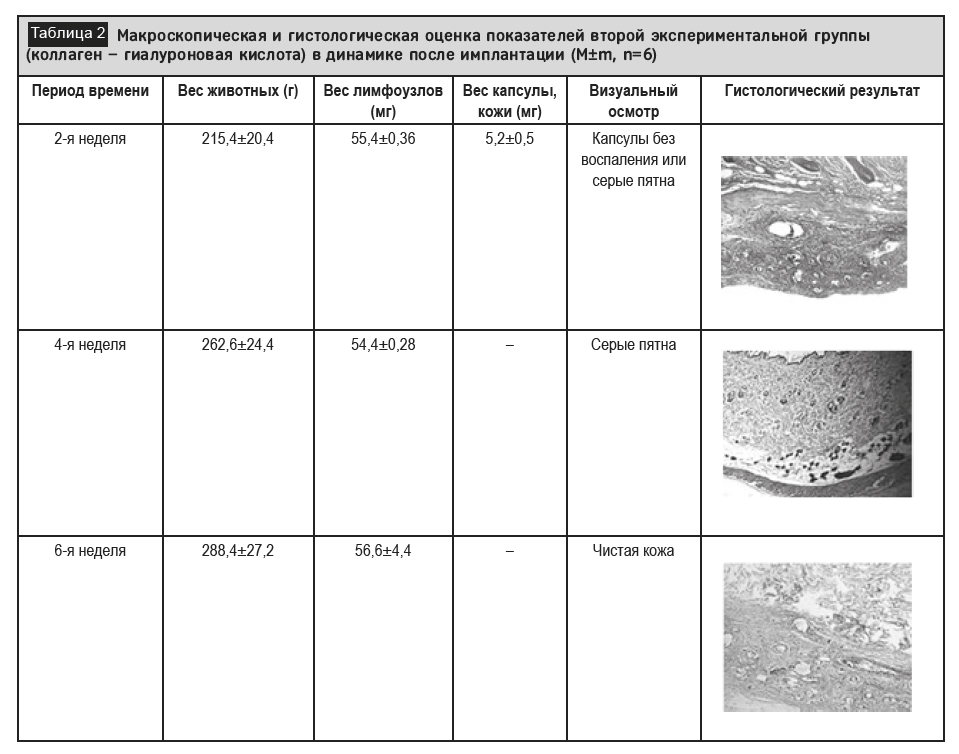
Масса животных во второй экспериментальной группе (коллаген – гиалуроновая кислота) увеличилась в 1,22 раза к 4-й неделе и в 1,34 раза к 6-й неделе относительно 2-й недели (215,4±20,4 г). Масса лимфоузлов снизилась в 0,98 раза на 4-й неделе и выросла в 1,02 раза на 6-й неделе по сравнению с исходным уровнем (55,4±0,36 мг). Масса капсулы и кожи на 2-й неделе составила 5,2±0,5 мг, при визуальном осмотре капсулы были чистыми, но с серыми пятнами на 4-й неделе и нормализацией к 6-й неделе.
Группа 2 (коллаген – гиалуроновая кислота) при гистологическом исследовании продемонстрировала более организованный и физиологический регенеративный ответ. На 2-й неделе грануляционная ткань характеризовалась упорядоченными коллагеновыми пучками и обильными функциональными сосудами с сохранением кожных придатков (табл. 2). К 4-й неделе сформировалась высокодифференцированная соединительная ткань в виде концентрических слоев параллельных коллагеновых пучков вокруг фрагментов имплантата с выраженной васкуляризацией и умеренной пролиферацией фибробластов. К 6-й неделе отмечалось благоприятная интеграция в регенеративном потенциале материала, при этом имплантат полностью замещался зрелой фиброзной тканью с сохраненной структурой дермы и сниженной васкуляризацией без гиалиновой трансформации.
Обсуждение
Настоящее исследование проясняет поведение резорбции и локальный тканевый ответ на коллагеновые композиты, модифицированные гидроксиапатитом и гиалуроновой кислотой, оцениваемые как биоактивные матрицы для регенеративных применений. Как показано в работе И.В. Майбородина и соавт. (2019), биодеградация коллагеновых мембран в мягких тканях преимущественно происходит в течение 4 недель при подкожной имплантации в моделях животных [2]. Резорбция коллагеновой губки происходит в процессе биодеградации. Этот процесс начинается с высвобождения металлопротеиназ матрицы (МПМ) клетками в хирургической зоне в рану во время заживления, за которым следует инфильтрация и колонизация матрицы фибробластами и капиллярами, приводящая к ремоделированию коллагенового каркаса и его замещению вновь синтезированной внеклеточной матрицей. Установлено, что продолжительность сохранения коллагенового композита играет ключевую роль в успехе регенеративных процедур [2, 12]. Согласно полученным данным, биодеградация модифицированных коллагеновых препаратов происходит в разные сроки в зависимости от модификации. К 4-й неделе композит «коллаген – гиалуроновая кислота» с минимальными геморрагиями полностью резорбировался, что доказывает высокую биодеградацию коллагена, в отличие от композита «коллаген – гидроксиапатит», который рассасывался дольше (4 недели) за счет минерального состава для остеокондукции, но с более интенсивной локальной геморрагической реакцией.
Исследования S. Gürbüz и соавт. (2023) также доказали, что при ЭПП и периапикальных дефектах применения мембраны «коллаген – гидроксиапатит», приводящий к увеличению объема регенерированной костной ткани, способствует улучшению клинического прогноза сохранения зубов [9]. Исследования G. Jain и соавт. (2018) также продемонстрировали, что применение бифазного кальций-фосфатного трансплантата Biograft-HT® в сочетании с коллагеновой мембраной Cologide™ способствует статистически значимому рентгенологическому заполнению костного дефекта и улучшению клинических параметров (CAL/PD) при лечении внутрикостных дефектов пародонта [10].
Исследования S. Lamichhane и соавт. (2023) показывают, что использование мембраны OSTEON™ III и Genoss collagen membrane безопасны в применении и обеспечивают положительное влияние на регенерацию пародонта при внутрикостных дефектах, демонстрируя прирост уровня клинического прикрепления десны на 2,1±1,25 мм, снижение глубины пародонтального кармана на 3,35±1,39 мм и рентгенологическое заполнение кости на 2,81±1,43 мм, несмотря на постоперационную рецессию десны [11].
Заключение
Проведенные результаты эксперимента подтверждают различия в профилях биодеградации, так как коллаген-гиалуроновый композит быстро резорбируется (4 недели) с минимальной тканевой реакцией, а коллаген-гидроксиапатит медленнее, проявляя остеокондуктивные эффекты. Эндопародонтальные поражения с проявлениями пародонтальных поражений для регенерации мягких тканей предпочтительно применение коллаген-гиалуроновой композиции, благодаря его высокой резорбции и благоприятному ответу. Экспериментальные эти материалы являются биосовместимыми, но требуют дальнейших рандомизированных клинических испытаний для внедрения в терапевтические протоколы.
ЛИТЕРАТУРА
1. Людчик Т.Б., Абдуллаев Ш.Ю., Муратова Н.Ю., и др. // Вестник современной клинической медицины. – 2023. – Т.16, Прил.2. – С.83–90.
2. Майбородин И.В., Хоменюк С.В., Михеева Т.В. и др. // Трансляционная медицина. – 2019. – №6(5). – С.55–67.
3. Моисеев Д.А., Румянцев В.А., Волков С.И., Кулюкина М.А., Конов А.А. // Проблемы стоматологии. – 2021. – №2. – С.77–83.
4. Моисеев Д.А., Копецкий И.С., Никольская И.А. и др. // Клиническая стоматология. – 2024. – №26(4). – С.18–28.
5. Юсупалиходжаева, С., Шомуродова, Г. // Стоматология. – 2023. – №1(1). – С.75–79.
6. Шомуродова Г.Х., Юсупалиходжаева С.Х. // Медицинский журнал Узбекистана. – 2017. – №1. – С.5–7.
7. Шомуродова Г.Х., Юсупалиходжаева С.Х. Ассоциация эндодонто-пародонтальных поражений системными заболеваниями.
8. Betancourt P., Elgueta R., Fuentes R. // Colomb Med (Cali). – 2017. – Vol.48, N4. – P.204–207.
9. Gürbüz S., Dogan A., Karakeçili A., Toközlü B. // Ulus Travma Acil Cerrahi Derg. – 2023. – Vol.29. – P.1081–1090.
10. Jain G., Dhruvakumar D., Wadhawan A. Comparative evaluation of efficacy of hydroxyapatite and ß-tricalcium phosphate (Biograft-HT®) with or without type 1 collagen membrane (CologideTM) in the treatment of intrabony defects in molars: A clinico-radiographic study. – 2018. – Vol.8, N1. – P.26.
11. Lamichhane S., Humagain M., Dawadi A., Rupakhety P. // Journal of Chitwan Medical College. – 2023. – Vol.13, N43. – P.64–71.
12. Tal H., Kozlovsky A., Artzi Z., Nemcovsky C.E., Moses O. // Clin Oral Implants Res. – 2008. – Vol.19, N8. – P.760–766.
13. Herrera D., Retamal-Valdes B., Alonso B., Feres M. // J Periodontol. – 2018. – Vol.89, Suppl.1. – S85–S102.
Медицинские новости. – 2026. – №3. – С. 83-86.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.