Внимание! Статья адресована врачам-специалистам
Sitnik A.A.
Republic Scientific-Practical Center of Traumatology and Orthopedics, Minsk, Belarus
Diagnostics and treatment of distal tibia fractures
Резюме. Переломы дистального отдела голени составляют 10% переломов нижней конечности и встречаются у молодых активных пациентов (30–40 лет) в результате высокоэнергетичной травмы. Тяжесть повреждений обусловлена незначительной толщиной мягкотканных покровов (высокая доля открытых повреждений и раневых осложнений в послеоперационном периоде), вовлечением суставной поверхности и возникновением дефектов кости вследствие вдавления. Традиционные методы хирургического лечения сопровождались раневыми осложнениями в 11–25% случаев, нарушениями консолидации до 9%, высокой частотой внутри- и околосуставных деформаций (до 42%). Понимание роли мягкотканных покровов, применение этапной тактики лечения (временная внешняя фиксация с окончательным остеосинтезом только после нормализации состояния мягких тканей через 12–21 сут) и методов минимально-инвазивного остеосинтеза, появление анатомически предызогнутых имплантатов с блокированием винтов позволили снизить частоту тяжелых осложнений.
Ключевые слова: дистальный отдел большеберцовой кости, малоберцовая кость, перелом, остеосинтез.
Summary. Distal tibia fractures comprise about 10% of all lower limb fractures and occur predominantly in young active people (30–40 y.o.) as a result of high-energy injury. The severity of injury depends on thin soft-tissue envelope (high percentage of open fractures and wound complications post-operatively), involvement of joint surface and bone defects due to impression. Traditional surgical treatment was accompanied by wound complications in 11–25% of cases, delayed and non-unions in 9%, intra- and periarticular malunions up to 42%. Understanding of the importance of soft-tissues, the introduction of staged treatment protocols (temporary external fixation and subsequent definitive fracture fixation only after soft-tissue recovery 12–21 days later), use of minimally-invasive fixation techniques and appearance of anatomically preshaped locked implants allowed to decrease the number of severe complications.
Keywords: distal tibia fracture, fibula, osteosynthesis.
Переломы дистального отдела большеберцовой кости составляют менее 10% всех переломов голени. Чаще повреждения возникают у мужчин, чем у женщин. Средний возраст пострадавших колеблется в пределах 35–40 лет. В последние десятилетия частота данных повреждений возрастает, что связано в первую очередь с ростом количества ДТП [3, 5, 10, 22]. Незначительная толщина мягкотканных покровов и сложность анатомии дистального отдела голени являются причиной высокой частоты осложнений и неудовлетворительных результатов при лечении этих повреждений.
Анатомические особенности
дистального отдела голени
Дистальная суставная поверхность большеберцовой кости имеет четырех-угольную форму и сочленяется с блоком таранной кости. Суставная поверхность шире спереди, чем сзади, является вогнутой в сагиттальной плоскости и слегка выпуклой во фронтальной плоскости. Медиально она ограничивается внутренней лодыжкой, латерально – вырезкой малоберцовой кости. Суставные поверхности лодыжек сочленяются с боковыми поверхностями блока таранной кости.
Большеберцовая и малоберцовая кости формируют дистально «вилку» голеностопного сустава. Одним из наиболее важных образований этого комплекса является дистальный межберцовый синдесмоз, фиксирующий малоберцовую кость в соответствующей вырезке большеберцовой кости. Более тонкая передняя межберцовая связка проходит от переднего бугорка большеберцовой кости (бугорок Chaput) дистально, кзади и латерально к передне-медиальному выросту на малоберцовой кости. Более мощная задняя синдесмозная связка включает lig. tibiofibulare posterius и lig. tibiofibulare transversale, которые простираются от заднего бугорка большеберцовой кости к заднему бугорку малоберцовой кости. Наконец, lig. tibiofibulare interosseum представляет собой утолщение межкостной мембраны.
Любое несоответствие отдельных компонентов в отношении длины, осевого положения и ротации приводит к локальным перегрузкам и последующему посттравматическому артрозу за счет преждевременного износа хрящевой поверхности [3, 8, 15].
Кровоснабжение дистального отдела большеберцовой кости осуществляется за счет множества сосудистых анастомозов, а не за счет какой-либо отдельной сосудистой ветви. При высокоэнергетичных переломах эта сосудистая сеть весьма уязвима, что сопровождается опасностью нарушения кровоснабжения кожи в зоне повреждения. Опасность ишемических повреждений кожи усугуб-ляется ранними хирургическими вмешательствами в данной зоне [17, 19].
Механизм повреждения
и патанатомия
Основным механизмом повреждения при переломах дистального метаэпифиза большеберцовой кости является осевое воздействие. При этом тяжесть повреждения может варьироваться от простых внутри- и околосуставных переломов до тяжелого раздробления суставной поверхности и метафиза (собственно перелом пилона).
В зависимости от положения стопы во время травмы, помимо компрессии, могут возникать эксцентрично действующие силы, вызывающие отрывные повреждения переднего или заднего края дистального отдела большеберцовой кости. При возникновении травмы в положении тыльного разгибания стопы определенную роль играет тяга икроножной мышцы (по типу стягивающей петли), которая препятствует смещению таранной кости кпереди и приводит к компрессии суставной поверхности большеберцовой кости [2].
Степень раздробления кости отражает величину воздействия, вызвавшего повреждение, и поэтому является косвенным показателем тяжести повреждения мягких тканей, которую иногда сложно оценить клинически в первые часы после травмы. Наиболее точно морфологию перелома можно оценить с помощью компьютерной томографии (КТ). При этом определяются шесть относительно постоянных костных фрагментов (рис. 1) [20]:
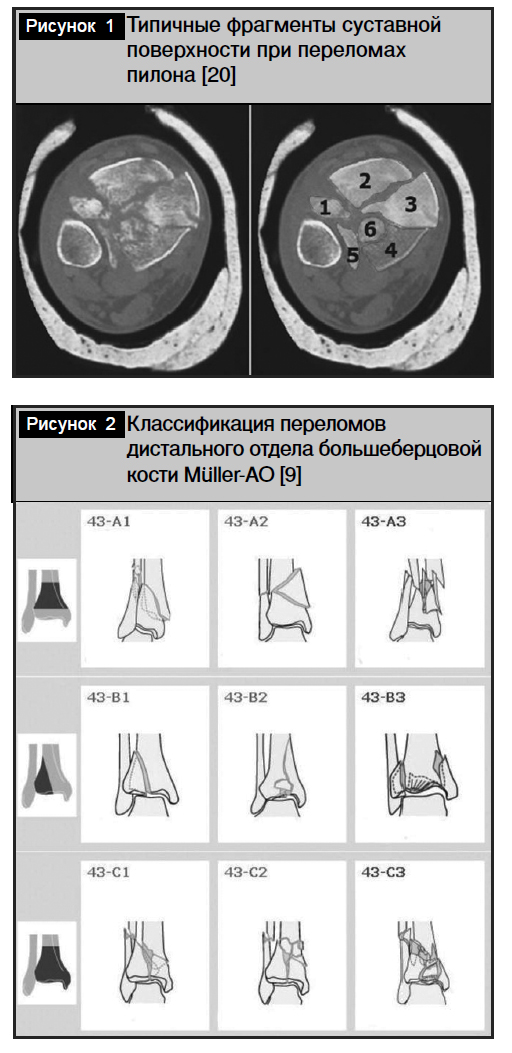
1) переднелатеральный фрагмент (имеется в 58% случаев) сохраняет связь с малоберцовой костью посредством передней синдесмозной связки;
2) передний фрагмент (76%) ограничивается сзади проходящей поперечно линией перелома;
3) фрагмент медиальной лодыжки (84%) может сохранять связь с передним или задним фрагментом; данный фрагмент может включать до 40% горизонтальной суставной поверхности большеберцовой кости;
4) задний фрагмент – аналог переднего фрагмента;
5) заднелатеральный фрагмент – самый мелкий, относительно редок (26%);
6) центральный фрагмент (50%) находится в центре зоны перелома и не имеет связи с остальной частью суставной поверхности; может составлять по размеру до 20% горизонтальной части суставной поверхности; для достижения хорошего результата необходима его точная репозиция.
Диагностика и классификация
Клиническая диагностика переломов дистального отдела большеберцовой кости не представляет сложностей в связи с выраженной болезненностью и деформацией сегмента конечности. При клиническом обследовании важно обращать внимание на состояние мягких тканей, выраженность отека, возможные нарушения периферического кровоснабжения и иннервации. Нередко данные повреждения возникают на фоне уже имеющихся поражений мягких тканей (трофические язвы, посттромбофлебитический синдром, варикозное расширение вен), что также необходимо учитывать.
При определенных механизмах травмы (ДТП, падение с высоты) следует подозревать и исключать другие повреждения. Нередко повреждениям дистального отдела голени сопутствуют переломы пяточной кости, мыщелков большеберцовой кости, таза и позвоночника.
Первым этапом инструментальной диагностики является рентгенография поврежденного сегмента в двух стандартных проекциях. Имеющееся при данных повреждениях укорочение сегмента препятствует четкой визуализации отдельных фрагментов перелома из-за их наложения друг на друга, поэтому рентгенограммы с вытяжением по оси более информативны. Рентгенологическая диагностика должна включать КТ, которая считается при данных повреждениях средством базовой диагностики. Особое значение имеют аксиальные срезы, позволяющие выявить степень фрагментации суставной поверхности. Выполнение 2D и 3D реконструкций значительно облегчает предоперационное планирование.
Классификация перелома должна учитывать его сложность, отражать прогноз и указывать возможные варианты лечения. На сегодняшний день общепринятой является классификация Müller-АО (рис. 2) [9]. В данной системе выделяется три типа переломов: тип А (внесуставные: целостность суставной поверхности не нарушена), тип В (неполные суставные: линия перелома проходит по суставной поверхности, но часть ее сохраняет связь с проксимальным отделом кости) и тип С (полные суставные переломы: линия перелома проходит через суставную поверхность и ее фрагменты не связаны с диафизом).
Состояние мягких тканей играет при переломах данной локализации важнейшую роль. Оно определяет не только возможность или невозможность открытой реконструкции суставной поверхности в ранние сроки после травмы (крайне высокая опасность раневых осложнений при обычно выраженном отеке мягких тканей), но и ряд отдаленных последствий, связанных с нарушением функции мышц, сухожилий и нервно-сосудистых образований данной области.
Для градации закрытых повреждений наибольшее распространение получила классификация Tscherne и Oestern [18], при открытых переломах не теряет своей актуальности классификация Gustilo и Andersen [6].
Методы лечения
Консервативное лечение. Консервативное лечение возможно лишь при переломах без смещения или при возможности достижения адекватной закрытой репозиции. Еще одним показанием может быть невозможность хирургического лечения (тяжелое общее состояние пациента, неудовлетворительное состояние мягких тканей в зоне повреждения, отказ пациента). Выполняется (при необходимости) закрытая репозиция перелома под наркозом с наложением глубокой гипсовой повязки, которая через 8–10 дней меняется на циркулярную. Иммобилизация продолжается в общей сложности до 8–12 недель в зависимости от типа перелома и данных промежуточных контрольных рентгенограмм. Следует помнить, что при многооскольчатых переломах суставной поверхности многие отломки теряют связь с мягкими тканями и не могут боль репонированы закрыто. Одними из характерных осложнений консервативного лечения являются вторичные смещения и посттравматические деформации [1, 10, 22].
Хирургическое лечение. Показания к хирургическому лечению при данных повреждениях:
– смещение суставных фрагментов;
– нестабильность сустава (подвывих/вывих таранной кости);
– нарушение оси конечности;
– открытые переломы.
Поскольку адекватное восстановление суставной поверхности может быть достигнуто только при прямой репозиции, в арсенале методов хирургического лечения переломов пилона длительное время доминировала открытая репозиция и внутренняя фиксация (ORIF), которая остается актуальной и на сегодняшний день с некоторыми оговорками (см. ниже).
Классический подход к открытой репозиции и внутренней фиксации при переломах дистального отдела голени, предложенный Rüedi и Allgower в 1969 г., включает четыре этапа [12]:
– остеосинтез малоберцовой кости;
– реконструкция суставного блока большеберцовой кости;
– костная пластика дефекта спонгиозной кости;
– фиксация суставного блока к диафизу большеберцовой кости.
1. Остеосинтез малоберцовой кости. При этом восстанавливается латеральная колонна голеностопного сустава и облегчается репозиция переднелатерального фрагмента большеберцовой кости. Так как для репозиции большеберцовой кости потребуется отдельный доступ, разрез кожи должен выполняться по заднему краю малоберцовой кости для сохранения максимально широкого кожного мостика между двумя доступами.
При репозиции малоберцовой кости не всегда требуется анатомичное восстановление ее длины. Важно восстановление длины относительно щели голеностопного сустава. При вальгусном смещении малоберцовой кости на нее воздействуют компрессионные силы. Поэтому для фиксации в таких случаях применяется более мощная 3,5 мм LC-DCP или LCP (она будет действовать как опорная пластина). При варусных смещениях на малоберцовую кость действуют силы растяжения, поэтому в таких случаях достаточно применения треть-трубчатой пластины в качестве нейтрализационной. При простых переломах малоберцовой кости возможна ее интрамедуллярная фиксация стержнем [5, 21].
2. Реконструкция суставного блока большеберцовой кости. Восстановление суставного блока при переломах пилона требует открытого доступа и может выполняться только после нормализации состояния мягких тканей, обычно не ранее 7–10 сут после травмы. При выполнении хирургического доступа следует учитывать, что он должен располагаться как минимум на расстоянии 7 см от доступа к малоберцовой кости для предотвращения ишемических повреждений кожного мостика. При планировании доступа следует оценивать данные КТ: желательно выходить на край костного отломка с целью минимизации оголения костных фрагментов.
Восстановление суставного блока обычно начинают с переднелатерального фрагмента. Его репонируют с помощью остроконечного зажима и временно фиксируют спицами Киршнера. Затем поочередно репонируются задний фрагмент, центральный фрагмент и также фиксируются спицами. Последним репонируют фрагмент внутренней лодыжки [10].
3. Костная пластика дефекта спонгиозной кости. При вдавлении фрагментов суставной поверхности за счет сминания спонгиозной костной ткани возникают дефекты в метафизе большеберцовой кости. Образующиеся после восстановления суставной поверхности пустоты требуют заполнения для предотвращения вторичного «проседания» суставной поверхности и обеспечения сращения. Наиболее часто для восстановления таких дефектов применяется (кортико-)спонгиозный аутотрансплантат из проксимального отдела большеберцовой кости или из крыла подвздошной кости. В последнее время все чаще применяют заменители костной ткани – резорбируемые костные цементы на основе фосфата кальция (Norian SRS, chronOS Inject, HydroSet и др.), что позволяет избежать выполнения второго доступа для забора трансплантата и связанных с этим осложнений. Применение имплантатов с блокированием винтов позволило несколько сократить необходимость костной пластики [1, 10, 19].
4. Фиксация суставного блока к диафизу большеберцовой кости. Чаще всего для достижения данной цели используются пластины, лишь в случаях недостаточной стабильности может применяться внешняя фиксация. Использование громоздких пластин для больших фрагментов (система 4,5 мм) при переломах данной локализации сопровождается чрезмерным натяжением краев кожи при ушивании раны. Поэтому более широкое применение находят пластины для малых фрагментов (треть-трубчатые пластины, Т-образные пластины для лучевой кости), а в последние годы – специальные пластины для дистального отдела большеберцовой кости с блокированием винтов (LCP). После ушивания раны рекомендуется применение гипсовой повязки с фиксацией стопы в правильном положении до заживления кожной раны и восстановления мышечного тонуса.
К сожалению, одновременное выполнение всех описанных этапов сопровождалось высокой частотой раневых осложнений – до 25% [11, 17]. Необходимы были изменения хирургической тактики (большее внимание состоянию мягких тканей) и совершенствование имплантатов.
В настоящее время все более широкое распространение находит тактика этапного лечения данных повреждений. При этом первым этапом производится наложение стержневого аппарата с целью мостовидной фиксации голеностопного сустава и, при необходимости и при возможности, выполнение погружного остеосинтеза малоберцовой кости (состояние мягких тканей!). Второй этап лечения – окончательный остеосинтез дистального отдела большеберцовой кости – выполняется через 7–10 сут (и более) после стабилизации состояния мягких тканей [2, 13].
Применяемые доступы
Стержневой аппарат. В большеберцовую кость устанавливают два винта Schanz по переднемедиальной поверхности на достаточном отдалении от зоны повреждения и от зоны выполнения последующего погружного остеосинтеза. Через пяточную кость поперечно проводится трансфиксирующий (сквозной) стержень. Стержни соединяются между собой с формированием «дельта»-рамы внешнего фиксатора. При выраженной нестабильности перелома такая фиксация может дополняться введением стержней меньшего диаметра в I (и V) плюсневые кости для предотвращения эквинусной деформации стопы (рис. 3) [13].
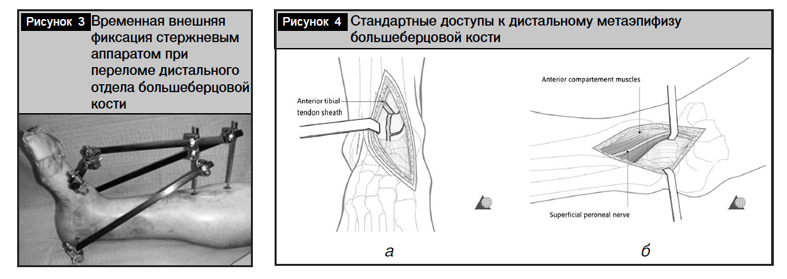
Для остеосинтеза малоберцовой кости применяется наружный доступ. Чтобы между двумя разрезами (медиальным и латеральным) оставался кожный мостик шириной не менее 7 см, доступ к малоберцовой кости располагают чуть кзади.
Стандартными доступами для остеосинтеза дистального отдела большеберцовой кости являются переднемедиальный и переднелатеральный (рис. 4) [4, 19].
Переднемедиальный доступ (рис. 4, а) начинается на 5–8 см проксимальнее щели голеностопного сустава, латеральнее гребня большеберцовой кости и проходит прямо над голеностопным суставом в направлении основания ладьевидной кости по медиальному краю сухожилия передней большеберцовой мышцы. Это обеспечивает лучший доступ к передней части большеберцовой кости, чем изогнутый разрез [4]. Следует избегать формирования кожных лоскутов латерально; для предотвращения любых дополнительных нарушений кровоснабжения фрагментов перелома важно минимальное их оголение и бережное обращение с надкостницей. Голеностопный сустав вскрывается в том же (вертикальном) направлении. Любые поперечные разрезы передней части капсулы для дальнейшего обнажения сустава должны сводиться к минимуму, так как это создает опасность деваскуляризации передних фрагментов (снабжаемых ветвями передней большеберцовой артерии). Разведение переднемедиального и переднелатерального суставных фрагментов с помощью пластинчатого расширителя обнажает сустав и обеспечивает доступ к центру перелома [10].
Переднелатеральный доступ к большеберцовой кости в некоторых случаях позволяет фиксировать и малоберцовую кость. Кожный разрез проводится между передним краем малоберцовой кости и большеберцовой костью в проекции переднелатерального угла большеберцовой кости (бугорок Tilleaux–Chaput). Рассекают удерживатель разгибателей, а передний большеберцовый сосудисто-нервный пучок отводят медиально. Суставную капсулу рассекают вертикально между переднелатеральным и передним суставными фрагментами (рис. 4, б).
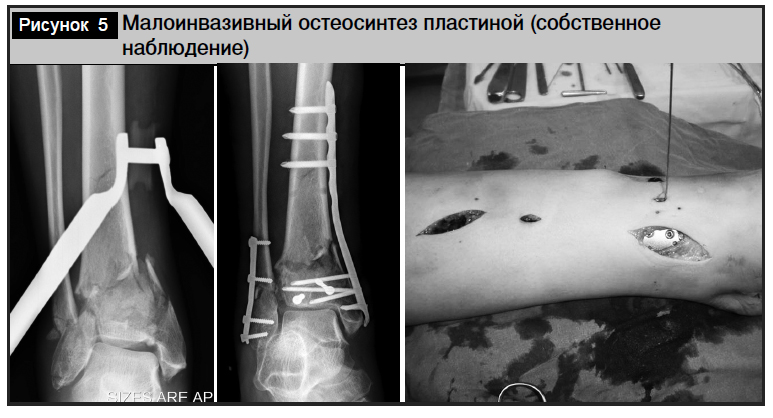
Малоинвазивный остеосинтез. Длина разреза должна быть достаточной для адекватной прямой репозиции суставных фрагментов, однако обнажение и анатомичная репозиция метадиафизарной зоны в настоящее время не считается желательным. Поэтому с целью максимального сохранения периостального кровообращения в зоне перелома пластина может проталкиваться над костью проксимально и фиксироваться к диафизу из отдельного доступа или проколов кожи. Важным при этом является восстановление осевых соотношений (ось и ротация). Появление новых анатомически предызогнутых пластин с блокированием винтов для применения по медиальной или переднелатеральной поверхностям большеберцовой кости значительно облегчает такую фиксацию (рис. 5) [14].
Гибридная внешняя фиксация. При значительном раздроблении кости и выраженном повреждении мягких тканей анатомичная репозиция суставной поверхности может быть опасной и/или невозможной. В таких случаях для окончательного лечения перелома может применяться кольцевидный внешний фиксатор (Илизарова или гибридный спице-стержневой, рис. 6) [2].
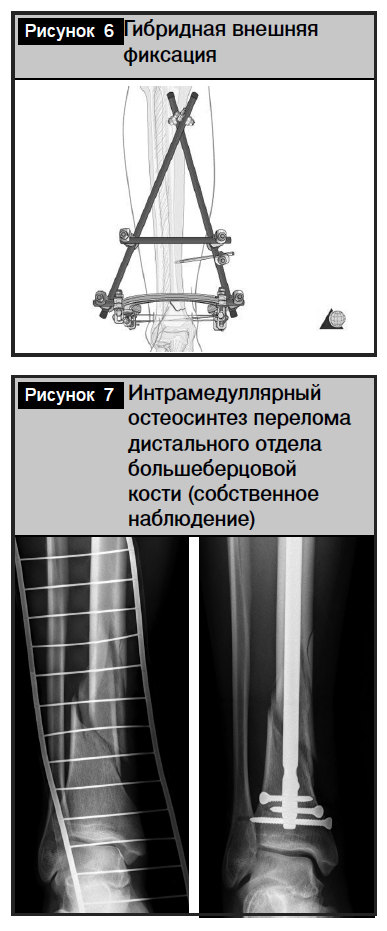
Интрамедуллярный остеосинтез. При некоторых относительно простых типах переломов дистального отдела большеберцовой кости с сохранением целостности суставного блока (43А) или возможностью его малоинвазивной реконструкции стягивающими винтами чрескожно (43С1, 43С2), для фиксации метадиафизарного перелома может применяться интрамедуллярный остеосинтез. При этом используются стержни с расширенными возможностями дистального блокирования: установка до блокирующих 5 винтов в дистальный фрагмент (рис. 7) [22].
Результаты лечения
Результаты после переломов пилона зависят от трех основных факторов [2, 17]:
– первичной тяжести повреждения, отражаемой в классификации перелома и повреждения мягких тканей;
– возможностей и опыта хирурга;
– пациента (общее состояние, состояние кровоснабжения, выполнение предписаний врача и т.д.).
Частота раневых осложнений по данным литературы колеблется в среднем от 11 до 14% [12], глубоких нагноений – от 2,5 до 10% (а при целенаправленном изучении в группах с тяжелыми повреждениями мягких тканей – до 22,2%) [11]. Нарушения консолидации отмечаются в 1,6–9% случаев, а при тяжелых повреждениях мягких тканей достигают 25% [11]. Важной проблемой остается сращение в неправильном положении с развитием внутрисуставных и внесуставных деформаций. По данным некоторых публикаций, частота таких осложнений достигала 42% [19], однако в последние годы с применением тактики этапного лечения ее удалось значительно сократить [13].
Сравнение результатов различных публикаций весьма затруднительно. Группы пациентов сильно различаются (частота и степень повреждений мягких тканей, доля сложных переломов), также отличаются и выполняемые оперативные вмешательства.
Несмотря на высокий уровень осложнений, в 60–80% случаев могут быть достигнуты хорошие отдаленные функцио-нальные результаты [1, 20, 21]. Имеется прямая зависимость между качеством анатомичного восстановления голеностопного сустава и хорошим результатом даже в отдаленные сроки [8, 15]. С другой стороны, рентгенологическая картина не всегда соответствует клиническим и функциональным результатам. Артродезы голеностопного сустава необходимы относительно редко (3–27%) и чаще всего связаны с развитием дегенеративных изменений [5]. Наилучшие функциональные результаты могут достигаться у пациентов с высокой степенью ответственности, более часто наблюдаемой у работающих не по найму, занимающихся спортом и социально интегрированных людей. Например, согласно результатам исследования, включавшего 112 человек, функциональные результаты были хорошими у 74,5% пациентов спустя 1 год после травмы и улучшались после среднего периода наблюдения в 10 лет (80,9%), хотя рентгенологически степень остеоартроза увеличивалась [15].
Таким образом, переломы дистального отдела голени представляют значительные сложности при лечении. Основной проблемой является состояние мягких тканей, которое определяет возможность и сроки выполнения хирургического лечения. Внедрение этапного подхода – временная иммобилизация (внешний фиксатор) с последующим отсроченным окончательным хирургическим лечениям после нормализации состояния мягких тканей (7–21-е сутки) – позволяет значительно снизить опасность раневых осложнений, а также улучшить отдаленные результаты лечения за счет более детального планирования фиксации с учетом данных дополнительных исследований (рентгенограммы с вытяжением, КТ). Долгосрочные результаты зависят от качества восстановления суставной поверхности и достижения сращения в анатомически правильном положении. Важную роль играет снижение хирургической травмы (малоинвазивная хирургия) и надежная фиксация фрагментов перелома (новые имплантаты с угловой стабильностью фиксации).
Л И Т Е Р А Т У Р А
1. Bastian L., Blauth M., Thermann H., Tscherne H. // Unfallchirurg. – 1995. – Vol. 98. – P. 551–558.
2. Bone L., Stegemann P., McNamara K. et al. // Clin. Orthop. – 1993. – Vol. 292. – P. 101–107.
3. Borelli J. Jr., Ellis E. // Orthop. Clin. N. Amer. – 2002. – Vol. 33. – P. 231–245.
4. Chen L., O’Shea K., Early J.S. // J. Orthop. Trauma. – 2007. – Vol. 21. – P. 207–211.
5. Crutchfield E.H., Seligson D., Henry S.L. et al. // Orthopedics. – 1995. – Vol. 18, N 7. – P. 613–617.
6. Gustilo R.B., Anderson J.T. // J. Bone Joint Surg. Am. – 1976. – Vol. 58. – P. 453–458.
7. Lau T.W., Leung F., Chan C.F., Chow S.P. // Int. Orthop. – 2008. – Vol. 32. – P. 697–703.
8. Marsh J.L., Weigel D.P., Dirschl D.R. // J. Bone Joint Surg. Am. – 2003. – Vol. 85, N 2. – P. 287–295.
9. Müller M.E., Nazarian S., Koch P. et al. The Comprehensive Classification of Fractures of Long Bones. – Berlin; Heidelberg; NewYork, 1990. – 680 p.
10. Newman S.D., Mauffrey C.P., Krikler S. // Injury. – 2011. – Vol. 42, N 10. – P. 975–984.
11. Rommens P.M., Claes L., De Boodt P. et al. // Unfallchirug. – 1994. – Vol. 97, N 1. – P. 39–46.
12. Rüedi T., Allgower M. // Injury. – 1969. – Vol. 1. – P. 92–99.
13. Sirkin M., Sanders R., Di Pascuale A. // J. Orthop. Trauma. – 1999. – Vol. 13. – P. 78–84.
14. Sitnik A., Beletsky A. // Clin. Orthop. – DOI 10.1007/s11999-013-2841-x (article in press).
15. Sommer C., Leutenegger A., Rüedi T. // Ned. Tijdschr. Traum. – 1998. – Vol. 3 (Suppl.). – P. 130.
16. Tornetta P.I. // Clin. Orthop. – 1996. – Vol. 323. – P. 273–276.
17. Trentz O., Friedl H.P. Critical softtissue conditions in pilon fractures // Major Fractures of the Pilon, the Talus, and the Calcaneus / H. Tscherne, J. Schatzker (eds.). – Berlin; Heidelberg; New York, 1993. – P. 59–64.
18. Tscherne H., Oestern H.J. // Unfallheilkunde. – 1982. – Vol. 85. – P. 111–115.
19. Teeny S., Wiss D.A. // Clin. Orthop. – 1993. – Vol. 292. – P. 273–276.
20. Tornetta P., Weiner L., Bergman M. et al. // J. Orthop. Trauma. – 1993. – Vol. 7, N 6. – P. 489–496.
21. Waddell J.P. Tibial plafond fractures // Major Fractures of the Pilon, the Talus, and the Calcaneus / H. Tscherne, J. Schatzker (eds.). – Berlin; Heidelberg; New York, 1993. – P. 43–48.
22. Zelle B.A., Bhandari M., Espiritu M. // J. Orthop. Trauma. – 2006. – Vol. 20, N 1. – P. 76–79.
Медицинские новости. – 2013. – №7. – С. 31-35.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.