Внимание! Статья адресована врачам-специалистам
Trisvetova E.L.
Belarusian State Medical University, Minsk
The clinical significance of heart rate regulation
with ivabradine in stable angina pectoris and chronic heart failure
Реферат. Частота сердечных сокращений относится к независимым факторам риска прогрессирования стабильной стенокардии и хронической сердечной недостаточности. Снижение частоты сердечных сокращений b-адреноблокаторами и недигидропиридиновыми блокаторами медленных кальциевых каналов не всегда успешно из-за нежелательных реакций препаратов. Ивабрадин является селективным ингибитором If-каналов в синусовом узле и отличается от других хронотропных препаратов, снижает скорость диастолической деполяризации и замедляет частоту сердечных сокращений, не вызывает снижения артериального давления и сократимости миокарда. Препарат рекомендован к применению при стабильной стенокардии, хронической сердечной недостаточности у пациентов с синусовым ритмом и частотой сердечных сокращений более 70 ударов в минуту. Помимо оригинального ивабрадина в настоящее время успешно применяют дженерический – «Раеном»® (ОАО «Гедеон Рихтер», Венгрия), сопоставимый по терапевтическому действию с оригиналом.
Ключевые слова: частота сердечных сокращений, стабильная стенокардия, хроническая сердечная недостаточность, ивабрадин.
Медицинские новости. – 2019. – №9. – С. 25–29.
Summary. Heart rate is an independent risk factor for the progression of stable angina and chronic heart failure. Decrease in heart rate with b-blockers and non-dihydropyridine blockers of slow calcium channels is not always successful due to undesirable drug reactions. Ivabradine is a selective inhibitor of If-channels in the sinus node and differs from other chronotropic drugs, reducing the rate of diastolic depolarization and slowing the heart rate, does not cause a decrease in blood pressure and myocardial contractility. The drug is recommended for use in stable angina, chronic heart failure in patients with sinus rhythm and heart rate of more than 70 beats per minute. In addition to the original drug ivabradine, they are now successfully using a generic drug – Raenom (Gedeon Richter).
Keywords: heart rate, stable angina, chronic heart failure, ivabradine.
Meditsinskie novosti. – 2019. – N9. – P. 25–29.
С появлением новых фармакологических средств, кардиохирургических и интервенционных методов достигнут определенный прогресс в лечении ишемической болезни сердца (ИБС). Вместе с тем распространенность ИБС не снижается, возрастает количество обращений и число госпитализаций пациентов по поводу обострения заболевания или прогрессирования хронической сердечной недостаточности [1]. Смертность от сердечно-сосудистых болезней сохраняет лидирующие позиции среди причин смертности от всех заболеваний во многих странах мира и Республике Беларусь [2, 3]. При изучении факторов риска развития и смертности от заболеваний сердечно-сосудистой системы, помимо артериальной гипертензии, дислипидемии, нарушений углеводного обмена, гиподинамии, выявили неблагоприятную роль повышения частоты сердечных сокращений (ЧСС) [2, 4]. Многие эпидемиологические исследования показали, что повышение ЧСС относится к независимым факторам риска заболеваемости и смертности у здоровых людей, при ИБС, атеросклеротическом поражении периферических артерий, хронической сердечной недостаточности [4, 5].
В клинических исследованиях BEAUTIFUL, INVEST, SHIFT доказана зависимость между ЧСС и риском неблагоприятного исхода. В первом исследовании при ЧСС выше 70 ударов в минуту повышался риск кардиоваскулярной смерти, частота госпитализаций по случаю фатального и нефатального инфаркта миокарда, коронарного вмешательства [5]. Во втором исследовании у пожилых пациентов с ИБС и артериальной гипертензией определили ассоциацию повышения уровня ЧСС с повышением риска нежелательных реакций медикаментозной терапии [6]. В исследовании SHIFT уменьшение частоты смертельных исходов от сердечно-сосудистых причин и количества госпитализаций из-за обострения хронической сердечной недостаточности снизилось в группе пациентов с ЧСС 50–60 ударов в минуту, получавших стандартную терапию и ивабрадин [7].
Таким образом, влияние повышенной ЧСС на исходы сердечно-сосудистых заболеваний и улучшение прогноза в случае снижения уровня ЧСС отмечено во многих исследованиях [4, 5]. Селективное снижение ЧСС путем ингибирования If-каналов ивабрадином является фармакологическим методом, применение которого у пациентов со стабильной стенокардией и хронической сердечной недостаточностью одобрено для клинической практики [5, 8].
Физиологическое и патофизиологическое значение увеличения частоты сердечных сокращений при ИБС
ЧСС относится к наиболее лабильным показателям сердечно-сосудистой деятельности, зависящим от многих факторов. Среди причин повышения ЧСС в состоянии покоя более 90 ударов в минуту рассматривают усиленное влияние симпатоадреналовой системы, снижение влияния на сердечно-сосудистую систему парасимпатического отдела вегетативной нервной системы и прямое повреждающее воздействие неблагоприятных факторов (физических, химических, биологических) на клетки синусового узла [8].
Известно, что изменение ЧСС влечет за собой изменения силы сокращений, скорости развития напряжения, времени изометрического расслабления миокарда. В случае увеличения ЧСС происходит укорочение времени достижения максимального сокращения и ускорение расслабления сердца. В свою очередь, укорочение времени диастолического расслабления приводит к снижению конечного диастолического объема желудочка и уменьшению ударного объема. Поскольку известно, что кровенаполнение коронарных артерий осуществляется во время диастолы желудочков, сокращение времени диастолического расслабления сопровождается снижением коронарного кровотока и потребления миокардом кислорода [4, 8].
При тахикардии нагрузка давлением за счет повышения среднего артериального давления (АД) больше по сравнению с состоянием, при котором ЧСС остается в пределах нормальных значений. Вследствие увеличившейся нагрузки возрастает работа сердца, развивается компенсаторная гипертрофия миокарда и гладкомышечных клеток стенок артериол, увеличивается потребность в кислороде при прежней его доставке миокарду [8, 9].
На фоне тахикардии повышается активность эктопических очагов автоматизма и триггерной активности, обусловленной поздней деполяризацией, как следствие, у пациентов с ИБС понижается порог фибрилляции предсердий [10].
Роль повышенной ЧСС как фактора прогрессирования атеросклероза коронарных артерий отмечена в нескольких исследованиях [9, 11]. Считается, что высокая ЧСС в состоянии покоя индуцирует разрыв атеросклеротической бляшки в коронарной артерии и развитие ишемии миокарда.
Основные патофизиологические механизмы, влияющие на течение ИБС при повышении ЧСС, представлены на рисунке 1.
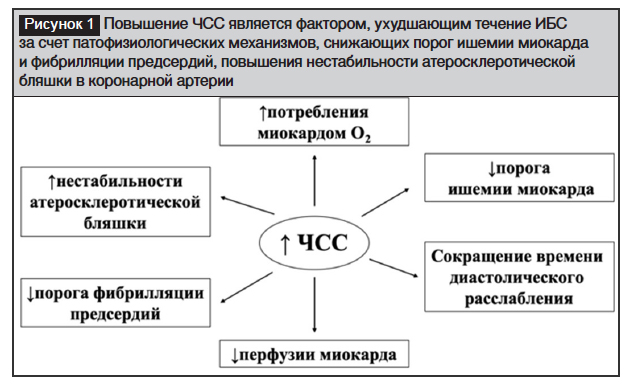
Начиная с Framingam Heart Study, известно, что ЧСС является самостоятельным фактором, оказывающим влияние на развитие осложнений течения ИБС и других сердечно-сосудистых заболеваний, тем самым влияющим на продолжительность жизни пациентов [12].
A. Diaz и соавт. проанализировали состояние большой группы пациентов (n=24 913) с подтвержденной ИБС за 14,7 года в зависимости от уровня ЧСС [13]. Авторы отметили повышение частоты случаев общей и сердечно-сосудистой смертности, госпитализаций у пациентов с ЧСС ≥83 ударов в минуту в состоянии покоя по сравнению с пациентами с ЧСС <83 ударов в минуту (р<0,0001). У пациентов с ЧСС в состоянии покоя ≥83 ударов в минуту на исходном уровне отметили более высокий риск общей смертности по сравнению с контрольной группой (ОR 1,32, ДИ 1,19–1,47; р<0,0001) и смертности от сердечно-сосудистых заболеваний (OR 1,31; ДИ 1,15–1,48, р<0,0001) после коррекции со множественными клиническими переменными.
Таким образом, доказательства неблагоприятного влияния повышенной ЧСС у пациентов с ИБС свидетельствуют о необходимости применения лекарственных препаратов, снижающих показатель до нормальных значений. Препараты первого ряда, рекомендованные для лечения ИБС (?-адреноблокаторы), снижают ЧСС, вместе с тем их применение ограничивают противопоказания. Многие клинические исследования показали, что снижение ЧСС достигается не у всех пациентов с ИБС, несмотря на использование ?-адреноблокаторов или недигидропиридиновых блокаторов медленных кальциевых каналов из-за нежелательных реакций [14, 15].
Фармакологические и гемодинамические свойства ивабрадина
Ингибитор токов ионных f-каналов в клетках синусового узла – ивабрадин – является первым селективным препаратом, уменьшающим скорость медленной спонтанной диастолической деполяризации и не влияющим на системное артериальное давление, сократимость миокарда и периферическое сопротивление сосудов. Известно, что f-каналы в клетках синусового узла, являясь основным регулятором скорости спонтанной диастолической деполяризации, активируются при гиперполяризации [16]. Специфическая селективная блокада токов f-каналов под действием ивабрадина приводит к уменьшению ЧСС в состоянии покоя и при активации симпатоадреналовой системы без дополнительного снижения АД. Ивабрадин оказывает антиишемический эффект у пациентов со стабильной стенокардией, сохраняя максимальный резерв дилатации коронарных артерий при физической нагрузке, увеличивая на 10% время диастолической перфузии коронарного русла, снижая потребность миокарда в кислороде (рис. 2) [17].
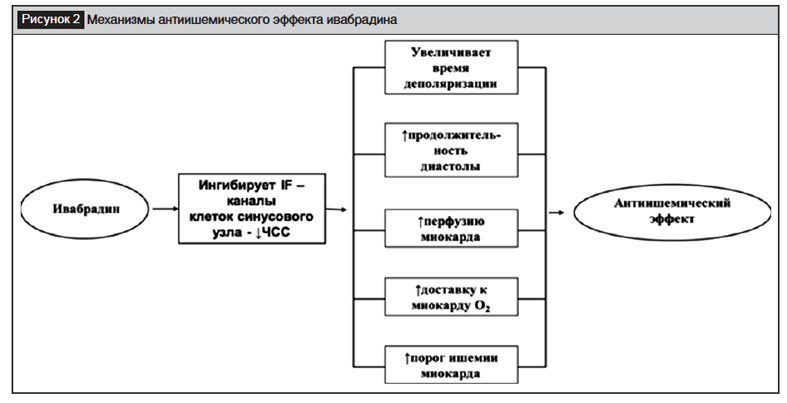
Ивабрадин после перорального приема быстро всасывается в кровь и достигает пиковой концентрации через 1–1,5 часа. При поступлении ивабрадина в организм человека образуется 22 метаболита в печени и кишечнике с участием фермента цитохрома Р450 3А4 (CYP3A4), метаболизм и концентрация в плазме которого не изменяются под влиянием препарата. Поскольку такие сильные ингибиторы фермента, как дилтиазем и верапамил, изменяют метаболизм цитохрома Р450 3А4 и концентрацию ивабрадина в плазме, их не применяют совместно с ивабрадином [18]. Основной период полураспада препарата составляет 2 часа, равновесная концентрация достигается в течение 24 часов, поэтому не отмечается накопления ивабрадина, так как он выводится из организма мочевыделительной системой и кишечником.
В физиологических условиях ЧСС определяется скоростью спонтанной диастолической деполяризации в синусовом узле, влияние на которую оказывает смешанный натриевый и калиевый ток, проходящий через f-каналы. Ивабрадин блокирует f-канал в открытом состоянии со стороны цитоплазмы, тем самым снижая частоту сокращений сердца. Препарат не оказывает непосредственного воздействия на трансмембранные натриевый и калиевый токи в кардиомиоцитах, клетки проводящей системы, не изменяет длительность интервала P-Q, Q-T, комплекса QRS. Блокирующее действие ивабрадина тем сильнее, чем выше ЧСС [19].
Специфичность ивабрадина для токов f-каналов объясняет отсутствие прямого влияния на функцию миокарда, реполяризацию желудочков и проводящую систему сердца. К тому же избирательность действия препарата ограничивает его применение при синусовом ритме и полностью исключает пациентов с фибрилляцией или трепетанием предсердий. Ивабрадин обладает высокой дозозависимостью: выраженный эффект наблюдают при высоких дозах и менее выраженный – при низких дозах препарата, при этом отмечают редкое (0,1%) развитие брадикардии [16].
При использовании ивабрадина нежелательные реакции (фотопсии, брадикардия, блокада сердца, головная боль) встречаются редко, противопоказаниями к назначению препарата являются низкая ЧСС (<70 ударов в минуту до начала лечения), индивидуальная непереносимость, тяжелая артериальная гипотензия (АД <90/50 мм рт. ст.), тяжелое заболевание печени, беременность, период грудного вскармливания. У пациентов в возрасте старше 75 лет следует рассматривать вопрос о применении более низкой стартовой дозы (2,5 мг два раза в сутки). Пациентам с почечной недостаточностью и клиренсом креатинина >15 мл/мин. коррекция дозы не требуется, при более тяжелой почечной недостаточности следует применять с осторожностью [2, 5].
Ивабрадин и стабильная стенокардия
Во многих клинических исследованиях показано, что снижение ЧСС под влиянием ивабрадина у пациентов со стабильной стенокардией сопровождается антиишемическим эффектом [15, 17, 18, 20]. Ивабрадин проявлял антиангинальное действие при сравнении с плацебо, ?-адреноблокатором, блокатором медленных кальциевых каналов в различных возрастных группах независимо от пола и сопутствующих заболеваний пациентов [20–22]. Исследователи на фоне лечения стандартной терапией и ивабрадином отмечали уменьшение частоты приступов стенокардии, количества принимаемых таблеток нитроглицерина, повышение толерантности к физической нагрузке. Доказательства антиишемического действия ивабрадина получены при наблюдении за 5000 пациентов в рандомизированных клинических исследованиях и 11 000 пациентов со стабильной стенокардией в открытых наблюдательных исследованиях [18].
Антиишемический эффект ивабрадина у пациентов со стабильной стенокардией исследован при монотерапии и в сочетании с ?-адреноблокаторами.
J.S. Borer и соавт. в плацебо-контролируемом рандомизированном исследовании у 360 пациентов со стабильной стенокардией, получавших в течение 3 месяцев стандартную терапию и ивабрадин, исследовали переносимость физической нагрузки [20]. В зависимости от применяемой дозы ивабрадина (2,5; 5; 10 мг в сутки) наблюдали дозозависимое улучшение толерантности к физической нагрузке и удлинение времени до появления признаков ишемии миокарда на ЭКГ (депрессия сегмента ST на 1,0 мм) в отличие от группы, получавшей плацебо. За время лечения ивабрадином количество приступов стенокардии в неделю снизилось с 4,14 до 0,95 (р<0,001), использование нитратов короткого действия – с 2,28 до 0,5 таблетки в неделю (р<0,001). Исследователи отметили антиишемическую и антиангинальную эффективность ивабрадина и его безопасность в течение времени наблюдения.
S. Perings и соавт. наблюдали 1250 пациентов в возрасте 66,0±10,9 года (мужчины (59,6%) и женщины, перенесшие инфаркт миокарда) со стенокардией напряжения и показаниями для назначения ивабрадина [23]. Большинство пациентов (65%) в составе стандартной терапии (ингибиторы АПФ/блокаторы рецепторов ангиотензина II, блокаторы медленных кальциевых каналов, диуретики, нитраты длительного действия, дезагреганты, статины) получали ?-адреноблокаторы. На фоне лечения ивабрадином в средней суточной дозе 11,0±2,7 мг, продолжавшегося в течение 4 месяцев, ЧСС снизилась с 82,4±11,8 до 67,1±8,4 удара в минуту (рис. 3).
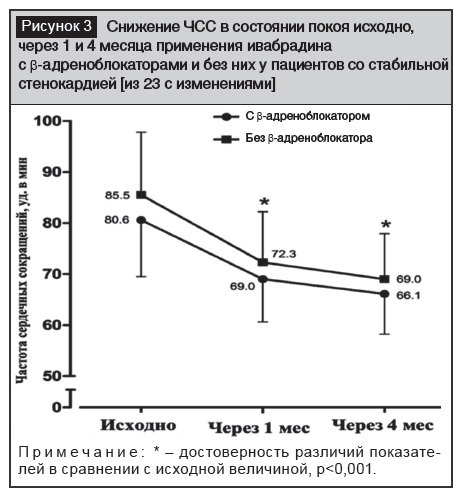
Авторы отметили, что среднее количество приступов стенокардии в неделю у пациентов снизилось с 1,2±1,9 до 0,1±0,6, сократилось количество принимаемых таблеток нитроглицерина (рис. 4). Сочетание ивабрадина с ?-адреноблокатором усиливало влияние на ЧСС и не вызывало нежелательных реакций препаратов.
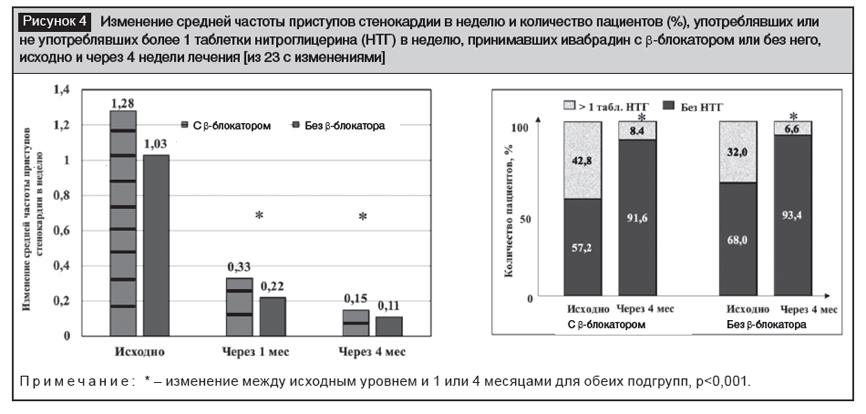
Сложные механизмы антиишемического действия ивабрадина включают снижение ЧСС и положительное влияние на окислительный стресс и функцию эндотелия.
Изучение функции эндотелия в клиническом исследовании у пациентов с ИБС после полной реваскуляризации методом чрескожной коронарной ангиопластики (ЧКВ), получавших ивабрадин, выполнено в 2015 году [24]. Пациенты через 70 дней после ЧКВ рандомизированы на две группы: в первой (n=36) – к стандартной терапии добавляли ивабрадин 5 мг 2 раза в день, во второй (n=34) – продолжили стандартную терапию. Через 4 недели дозу ивабрадина увеличивали до 7,5 мг 2 раза в день при ЧСС >60 ударов в минуту в состоянии покоя и продолжали наблюдение последующие 4 недели. Оценивали эндотелийзависимую и эндотелийнезависимую функции пробой с реактивной гиперемией. В течение периода исследования отметили значительное снижение ЧСС в обеих группах, а улучшение поток-зависимой вазодилатации – только в первой группе, получавшей ивабрадин. Таким образом, помимо снижения ЧСС ивабрадин улучшает функцию эндотелия у пациентов с ИБС после ЧКВ.
Сравнительное исследование эффективности и безопасности оригинального препарата ивабрадина («Кораксан»?, Сервье) и дженерического («Раеном»?, Гедеон Рихтер) выполнено у пациентов со стенокардией напряжения II–III функционального класса [25]. В исследование включили 20 пациентов с ЧСС более 70 ударов в минуту, несмотря на прием ?-адреноблокатора, у которых помимо ИБС диагностировали артериальную гипертензию 1–3 степени и хроническую сердечную недостаточность I–III функционального класса. В первой группе к стандартной терапии добавляли Кораксан и наблюдали в течение 4 недель, Кораксан заменяли препаратом «Раеном»? и наблюдали еще 4 недели. Пациентам второй группы коррекцию частоты сердечных сокращений начинали с назначения препарата «Раеном»? в течение 4 недель, который, наоборот, заменяли Кораксаном и наблюдали в течение такого же срока.
Результаты пилотного исследования небольшой группы пациентов показали сопоставимый терапевтический эффект оригинального и дженерического препаратов. В обеих группах к концу четвертой недели исследования достигнуто снижение частоты сердечных сокращений: в 1-й группе – 66,3±6,18 против 82,5±6,63; во 2-й группе – 67,6±5,97 против 83,0±6,18 ударов в минуту; p<0,01 для обеих групп. Авторы отметили на фоне снижения ЧСС уменьшение количества еженедельных приступов стенокардии и принимаемых для их купирования таблеток нитроглицерина. Сравнение степени изменения изучаемых параметров в процессе лечения не выявило статистически значимых отличий между наблюдаемыми группами пациентов. За период исследования не наблюдали нежелательных реакций на Кораксан? и Раеном?.
Антиишемическая и антиангинальная эффективность ивабрадина подтверждает рекомендуемое применение препарата для симптоматического лечения пациентов со стабильной стенокардией в виде монотерапии или в комбинации с ?-адреноблокаторами. В случае комбинации ?-адреноблокаторов с ивабрадином отмечают дополнительное снижение ЧСС, уменьшение частоты симптомов стенокардии и эпизодов ишемии миокарда, повышение переносимости физических нагрузок, улучшение качества жизни [26].
Европейское агентство по лекарственным препаратам (EMA) в 2005 году одобрило применение ивабрадина при стабильной стенокардии, в 2012 году, принимая во внимание результаты рандомизированных контролируемых исследований, в показания к назначению ивабрадина включили пациентов с систолической сердечной недостаточностью и сниженной фракцией выброса (ФК II–IV, ФВ ЛЖ ≤35%, ЧСС ≥70 уд./мин.). Управление по контролю за продуктами и лекарствами США (FDA) в 2015 году также одобрило применение ивабрадина у пациентов с сердечной недостаточностью и сниженной фракцией выброса с ЧСС ≥70 уд./мин. на фоне применения максимальной переносимой дозы ?-адреноблокаторов или при противопоказаниях к назначению последних [27].
Хроническая сердечная
недостаточность
Известно неблагоприятное влияние высокой ЧСС при хронической сердечной недостаточности с сохраненной или сниженной фракцией выброса, а также эффективность b-адреноблокаторов в снижении заболеваемости и смертности пациентов. Нежелательные реакции (гипотензия, усталость, брадикардия и т.п.) и противопоказания (бронхиальная астма, усиление бронхообструктивного синдрома при заболеваниях легких) ограничивают применение ?-адреноблокаторов, поэтому эффект в лечении достигается комбинированием или использованием монотерапии ивабрадином.
Проспективное когортное амбулаторное исследование эффективности и безопасности ивабрадина при хронической сердечной недостаточности и сниженной фракцией выброса выполнено у 767 пациентов [16]. В течение 12 месяцев пациенты с ЧСС ≥70 уд./мин. 2 раза в день получали ивабрадин дополнительно к стандартной терапии, в том числе ?-адреноблокаторами в 65% случаев. К концу наблюдения (в среднем 11,2 месяца) терапию ивабрадином продолжали 90% пациентов. Через год лечения ЧСС снизилась по сравнению с исходным значением на 16 уд./мин., улучшился функцио-нальный класс (NYHA), снизилась частота обострений сердечной недостаточности с 36% до 8%. Авторы отметили повышение фракции выброса левого желудочка (+5,1% в течение года), снижение BNP и доли пациентов, госпитализированных по поводу обострения хронической сердечной недостаточности (с 23% до 5%). Нежелательные реакции наблюдали у 3% пациентов, что соответствовало профилю безопасности препарата.
В рекомендациях ACC/AHA и ESC ивабрадин отмечен как препарат для снижения частоты госпитализаций по поводу сердечной недостаточности у пациентов со стабильной стенокардией напряжения ФК II–III (NYHA) и хронической сердечной недостаточностью со сниженной фракцией выброса, синусовым ритмом и ЧСС ≥75 уд./мин., получающих стандартную терапию и имеющих ограничения или противопоказания для ?-адреноблокаторов (класс IIa) [28, 29].
Заключение
Уникальные электрофизиологические свойства, проявляющиеся отрицательным хронотропным влиянием на синусовый узел и отсутствием клинически значимых других эффектов, позволяют рассматривать назначение ивабрадина в комплексной терапии как возможность повышения эффективности лечения стабильной стенокардии и систолической хронической сердечной недостаточности. Выполненные к настоящему времени исследования доказали эффективность и безопасность ивабрадина в лечении разных групп пациентов со стабильной стенокардией и хронической сердечной недостаточностью со сниженной фракцией выброса и коморбидными состояниями, включающими артериальную гипертензию, ожирение, метаболический синдром, сахарный диабет. Создание дженерического препарата «Раеном»?, сопоставимого по действию с оригиналом, расширяет возможности пациентов в выборе оптимального лечения стабильной стенокардии и хронической сердечной недостаточности.
Л И Т Е Р А Т У Р А
1. Bhatnagar P., Wickramasinghe K., Wilkins E., et al. // Heart. – 2016. – Vol.10, N24. – P.1945–1952.
2. Montalescot G., Udo Sechtem U., Achenbach S., et al. // Eur. Heart J. – 2013. – Vol.34. – P.2949–3003.
3. Диагностика и лечение стабильной стенокардии. Национальные рекомендации. – Минск, 2010.
4. Pocock S.J., Wang D., Pfeffer M.A., et al. // Eur. Heart J. – 2006. – Vol.27. – P.65–75.
5. Fox K., Ford I., Steg P.G., et al. // Lancet. – 2008. – Vol.372. – P.817–21.
6. Pepine C.J., Handberg E.M., Cooper-DeHoff R.M., et al. // JAMA. – 2003. – Vol.290, N21. – P.2805.
7. Böhm M., Borer J., Ford I., et al. // Clin. Res. Cardiol. – 2013. – Vol.102, N1. – P.11–22.
8. Heusch G. // Br. J. Pharmacol. – 2008. – Vol.153. – P.1589–1601.
9. Reil J.C., Custodis F., Swedberg K., et al. // Clin. Res. Cardiol. – 2011. – Vol.100. – P.11–19.
10. Lombardi F. // Eur. Heart J. – 1999. – Vol.1 (Suppl.H). – H44–H51.
11. Beere P., Glagov S., Zarins C. // Science 1984. – Vol.226. – P.180–182.
12. Kannel W.B., Kannel C., Paffenbarger R.S., et al. // Am. Heart J. – 1987. – Vol.113. – P.1489–1494.
13. Diaz A., Bourassa M.G., Guertin M.C., et al. // Eur. Heart J. – 2005. – Vol.26, N10. – P.867–874.
14. Tendera M., Fox K., Ferrari R., et al. // Int. J. Cardiol. – 2014. – Vol.176. – P.119–24.
15. Steg P.G., Ferrari R., Ford I., et al. // PLoS One. – 2012. – Vol.7, N5. – e36284.
16. Koruth J.S., Lala A., Pinney S., et al. // JACC. – 2017. – Vol.70, N14. – P.1777–1784.
17. Deedwania P. // Drugs. – 2013. – Vol.73. – P.1569–1586.
18. Kaski J.C., Gloekler S., Ferrari R., et al. // Open Heart. – 2018. – Vol.5. – e000725.
19. Savelieva I., Camm A.J. // Drug Saf. – 2008. – Vol.31. – P.95–107.
20. Borer J.S., Fox K., Jaillon P., et al. // Circulation. – 2003. – Vol.107. – P.817–823.
21. Tardif J.C., Ford I., Tendera M., et al. // Eur. Heart J. – 2005. – Vol.26. – P.2529–2536.
22. Ruzyllo W., Tendera M., Ford I., et al. // Drugs. – 2007. – Vol.67. – P.393–405.
23. Perings S., Stöckl G., Kelm M. // ADV Ther. – 2016. – Vol.33, N9. – P.1550–1564.
24. Mangiacarpra F., Colaiori I., Riccottini E., et al. // Clin. Res. Cardiol. – 2017. – Vol.106, N1. – P.69–75.
25. Поветкин С.В., Лунева Ю.В. // Рац. фармакотер. в кард. – 2018. – Vol.14, N1. – P.34–39.
26. Werdan K., Ebelt H., Nuding S., et al. // Cardiology. – 2016. – Vol.133. – P.83–90.
27. Zugck C., Störk S., Stöckl G. // Int. J. Cardiol. – 2017. – Vol.240. – P.258–264.
28. Shen W.K., Sheldon R.S., Benditt D.G., et al. // J. Am. Coll. Cardiol. – 2017. – Vol.70. – P.620–663.
29. Ponikowski P., Voors A.A., Anker S.D., et al. // Eur. J. Heart Fail. – 2016. – Vol.18. – P.891–975.
Медицинские новости. – 2019. – №9. – С. 25-29.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.