Mokhort T.V
Belarusian State Medical University, Minsk
Glucovance: new possibilities of antihyperglycemic therapy
Резюме. Изложены вопросы потенциальной оптимизации антигипергликемической терапии сахарного диабета 2-го типа с позиций оптимизации переносимости, комплаенса и стоимости лечения. Обоснована целесообразность использования комбинированной терапии для достижения целевых показателей углеводного обмена.
Ключевые слова: сахарный диабет 2-го типа, антигипергликемическая терапия, глюкованс.
Медицинскиеновости. – 2013. – № 11. – С. 57–61.
Summary. The issues of potential optimization of antihyperglycemic therapy in type 2 diabetes mellitus are discussed in the article (including tolerance optimization, compliance and the cost of treatment). The advisability of combined therapy to achieve target indices of carbohydrate metabolism is justified.
Keywords: type 2 diabetes mellitus, antihyperglycemic therapy, glucovance.
Meditsinskie novosti. – 2013. – N 11. – P. 57–61.
За последние десятилетия достигнут значительный прогресс в понимании механизмов развития, принципов диагностики, профилактики и терапии сахарного диабета 2-го типа (СД 2) – одного из наиболее распространенных неинфекционных заболеваний. Однако эти достижения далеко не всегда могут быть реализованы в полной мере в клинической практике, что не позволяет добиться желаемой эффективности лечения, основанного на знании патогенетических механизмов развития заболевания.
По данным Национального исследования здоровья и питания (National Health and Nutrition Examination Survey (NHANES) за 2003–2004 годы, 43% пациентов с СД, проживающих в США, не достигают целевых значений компенсации и имеют уровень HвA1c более 7%. По сравнению с 1999–2000 годами, последний результат демонстрирует положительную динамику и увеличение доли компенсированных пациентов с 37 до 67% [18].
В Республике Беларусь, по данным наблюдения М.Г. Русаленко (2008), установлено достижение целевых уровней контроля СД 1-го типа лишь у 18,2% взрослых пациентов. Декомпенсацию СД 1 определяют неадекватный самоконтроль, отсутствие навыков в коррекции дозы инсулина и ранняя манифестация заболевания, т.е. погрешности в выполнении рекомендаций по лечению [2]. В исследовании [1] компенсация СД 1 была достигнута у 23% пациентов.
Одна из причин недостаточной эффективности лечения СД – невыполнение рекомендаций врача. В частности, в центре внимания врачей остается несоблюдение режима питания и лечения. Недостаточная приверженность пациентов к лечению особенно актуальна при хронических заболеваниях, в число которых входит СД 2. По данным ВОЗ, до 50% пациентов с хроническими неинфекционными заболеваниями, включая СД 2, нарушают режим лечения и вовсе самостоятельно прерывают его [3]. Низкая приверженность к лечению входит в число основных причин снижения терапевтического эффекта, существенно повышает вероятность недостижения целевых показателей компенсации и, соответственно, развития хронических инвалидизирующих осложнений, что ведет к снижению качества жизни и последующему увеличению затрат на лечение.
Как мотивировать больных к выполнению назначений? Можно ли повысить приверженность пациентов к лечению так, чтобы существенно улучшились его конечные результаты?
Принципиально более активное привлечение пациента к лечению позволит обеспечить достижение компенсации заболевания и в итоге будет способствовать предупреждению развития и прогрессирования хронических осложнений. Данная модель рекомендаций поведения привела к появлению в литературе вместо привычного термина «compliance» (комплаенс, пер. с англ. – подчинение, податливость) терминов «concordance» (конкорданс, согласие) и «adherence» (соблюдение рекомендаций). Если модель отношения врача и пациента по типу «compliance» предусматривает пассивное подчинение врачу и простое выполнение пациентом врачебных инструкций, то модель «concordance» рассматривает процесс терапии как сотрудничество (партнерство) врача и пациента с активным вовлечением больного в процесс лечения [3]. Такое сотрудничество может быть обеспечено только в условиях достаточной информированности пациента о влиянии заболевания на здоровье и психологическую адаптацию. С целью повышения уровня знаний по проблеме диабета в Республике Беларусь успешно реализуется программа обучения пациентов в «школах диабета» с привлечением психотерапевта. К сожалению, пациенты не всегда понимают необходимость обучения, да и качество обучения в «школах диабета» нуждается в улучшении.
Второй путь, позволяющий оптимизировать достижение компенсации заболевания, – терапия с минимизаций количества приемов лекарственных препаратов. При СД 2 этот подход особо актуален, так как пациенту нужно принимать антигипергликемические, гипотензивные, гиполипидемические и другие препараты. В качестве альтернативы рекомендуются комбинированные препараты, например для антигипергликемического лечения могут быть использованы следующие комбинации:
– метформин + производные сульфонилмочевины;
– метформин + тиазолидиндионы;
– производные сульфонилмочевины + тиазолидиндионы;
– производные сульфонилмочевины + акарбоза;
– метформин + ингибитор дипептидил-пептидазы-4.
Наиболее часто используется двойная фиксированная комбинация метформина (500 мг) и производного сульфонилмочевины глибенкламида (2,5 или 5 мг) в препарате «Глюкованс». Выбор составляющих комбинации обусловлен основными патогенетическими характеристиками развития СД 2: инсулинорезистентности (ИР) и прогрессирующего снижения секреции инсулина. На рис. 1 представлены классические данные по эволюции ИР и динамике инсулиновой секреции при длительном течении СД 2, определяющие целесообразность двойной комбинации антигипергликемической терапии с воздействием на ИР (метформин) и снижение секреции инсулина (глибенкламид).
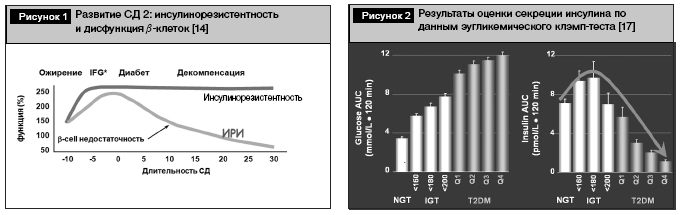
Инсулинорезистентность – биологический ответ периферических тканей организма на воздействие инсулина; при развитии СД 2 проявляется до манифестации заболевания и определяется влиянием ряда эндогенных, или генетических, и экзогенных факторов, приводящих к развитию ИР, включая нерациональное питание с развитием висцерального ожирения, дислипидемии, артериальной гипертензии, нарушений углеводного обмена. Именно висцеральное ожирение, являющееся маркером ИР, определяет глобальный рост заболеваемости СД 2 и включение метформина, как препарата, воздействующего на ИР, в рекомендации по лечению СД 2 во всех рекомендациях.
Метформин повышает чувствительность гепатоцитов и, в меньшей степени, миоцитов и адипоцитов к инсулину, положительно влияет на липидный обмен посредством уменьшения концентрации свободных жирных кислот и триглицеридов, замедляет всасывание углеводов из кишечника, что способствует уменьшению постпрандиальной гипергликемии, оказывает благоприятное действие на систему гемостаза, реологические свойства крови. Метформин не вызывает патологической прибавки массы тела, снижает риск гипогликемических эпизодов. Перечисленные эффекты метформина в итоге способствуют снижению риска сердечно-сосудистой патологии и микрососудистых осложнений СД. Доказано, что метформин стимулирует L-клетки кишечника и продукцию глюкагон-подобного пептида-1 [9], уменьшает накопление триглицеридов в печени, что определяет его эффективность в лечении неалкогольной жировой болезни печени [4], улучшает показатели эстроген-гестагенного статуса при синдроме поликистозных яичников [19, 24].
Второй важнейший фактор патогенеза СД 2 – дефекты секреции инсулина, проявляется в утрате или значительном снижении первой фазы глюкозоиндуцированной секреции инсулина, снижении или неадекватной стимуляции секреции инсулина, нарушении пульсаторной секреции инсулина, повышении секреции проинсулина, уменьшении секреции инсулина вследствие глюкозо- и липотоксичности. Так, в исследовании Сан-Антонио (The San Antonio Metabolism Study) и эпидемиологическом и генетическом исследовании (Veterans Administration Genetic Epidemiology Study) при использовании эугликемического клэмп-теста подтверждены нарушения инсулиновой секреции, обосновывающие возможность использования инсулиновых секретагогов [17] (рис. 2).
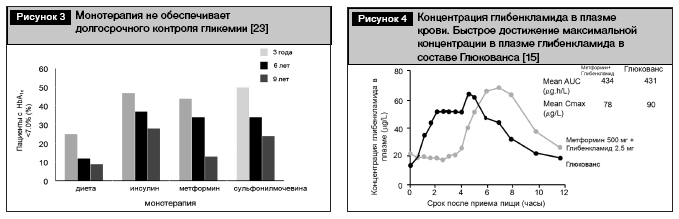
Приведенные факты обосновывают целесообразность использования комбинированной терапии метформином и производным сульфонилмочевины Глюковансом. Дополняют их факты, полученные в британском проспективном исследовании (рис. 3) и свидетельствующие о том, что монотерапия (диетотерапия, метформин или производные сульфонилмочевины) не обеспечивает долгосрочного контроля гликемии [24].
Доказательная база эффективности использования фиксированной комбинации метформина и глибенкламида – Глюкованса
Фармакокинетика метформина и глибенкламида позволяет принимать их одновременно 2 раза в сутки, хотя существуют некоторые технические трудности для объединения этих препаратов в одной таблетке. Глибенкламид плохо растворим, но хорошо всасывается из раствора в желудочно-кишечном тракте, поэтому его фармакокинетика определяется конкретной лекарственной формой. У больных, получающих микронизированную и обычную форму глибенкламида, существенно различается максимальная концентрация препарата в плазме крови. Биодоступность Глюкованса и свободной комбинации обоих компoнентов идентична. Фармакокинетика метформина неизменна, однако пик концентрации глибенкламида, включенного в Глюкованс благодаря уникальной системе доставки частиц глибенкламида разного размера (микронизированная форма), в плазме наступает раньше, что позволяет принимать препарат вместе с едой (рис. 4) [15].
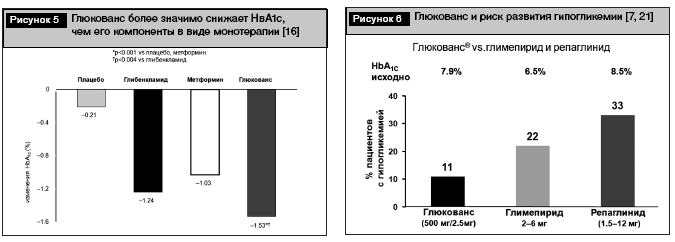
Глюкованс – это фиксированная комбинация метформина 500 мг и двух различных дозировок глибенкламида (2,5 или 5 мг) в одной таблетке. Глибенкламид в препарате «Глюкованс» представлен в микронизированной форме. Уникальная система доставки глибенкламида, который содержится в матриксе растворимого метформина в виде частиц строго определенного размера, способствует более быстрому его поступлению в кровоток после приема пищи (поэтому препарат можно принимать с едой) и обеспечивает меньший риск развития гипогликемии по сравнению с обычными препаратами глибенкламида и улучшенную переносимость. Доказано, что по сравнению с приемом отдельных компонентов препарат «Глюкованс» более значимо снижает уровнь не только глюкозы крови, но и НвА1с: на 1,53% против 1,24% в группе глибенкламида и на 1,03% в группе метформина (рис. 5) [16]. Следует отметить, что риск гипогликемических эпизодов в случае использования Глюкованса, глимепирида и репаглинида был минимальный в группе пациентов, принимавших Глюкованс, и максимальный в группе пациентов, принимавших репаглинид (рис. 6) [7, 21].
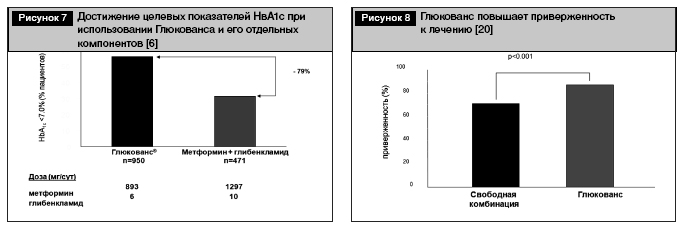
При проведении сравнительного анализа эффективности Глюкованса и приема комбинации двух препаратов – метформина и глибенкламида были получены результаты, свидетельствующие о предпочтительности приема Глюкованса. В результате доказано, что на 79% большее количество пациентов достигли уровня НвА1с <7.0% при использовании Глюкованса по сравнению с использованием отдельных компонентов препарата (рис. 7) [6].
Глюкованс снижает риск гипогликемий, лимитирующих использование секретагогов. Прием Глюкованса, обеспечивающий достижение целевых параметров компенсации, ассоциирован со снижением частоты легких и выраженных гипогликемических эпизодов. Например, в 52-недельном исследовании Blonde и соавт. при наблюдении за 477 пациентами, не достигшими целевых показателей углеводного обмена при монотерапии глибенкламидом, отмечено снижение частоты гипогликемических эпизодов при снижении НвА1с на 1,7% [5, 6]. Garber и соавт. при оценке эффективности Глюкованса в когорте 828 пациентов при равноценном снижении уровня НвА1с выявили, что частота гипогликемических эпизодов в целом была достаточно высокой – 19,9%, но ни один из пациентов с зарегистрированными гипогликемическими эпизодами не требовал медицинской помощи [16]. И, наконец, сравнительный анализ 2342 пациентов с СД 2, получавших лечение Глюковансом, проведенный Davidson и соавт., продемонстрировал различия в частоте гипогликемических эпизодов в различных исследованиях, что было обусловлено различиями в дизайне исследований и качестве оценки гипогликемических эпизодов. В итоге авторы сделали вывод о целесообразности использования Глюкованса, так как риск гипогликемических эпизодов, при сравнении с уровнем снижения гликемии, допустим [13].
Ретроспективный анализ также показал, что Глюкованс более эффективно снижает уровень HвA1c, чем совместное применение метформина и глибенкламида. Исследования показали, что при переводе больных с совместного применения метформина и глибенкламида на прием Глюкованса наблюдалось достоверное снижение уровня HbA1c (в среднем 0,6%), причем эффект был наиболее выражен у больных, имевших исходный уровень HbA1c больше 8%. Также продемонстрировано, что Глюкованс более эффективно контролировал постпрандиальный уровень гликемии, чем совместный прием глибенкламида и метформина [11, 12].
Комбинированная терапия метформином и препаратами сульфонилмочевины так же эффективна, как комбинированная терапия инсулином и препаратами сульфонилмочевины или монотерапия инсулином у пациентов с плохим эффектом от предшествовавшей терапии. Это подтверждается результатами перекрестного исследования 50 больных с СД 2 и вторичной резистентностью к препаратам сульфонилмочевины [22], которые были разделены на две группы. Пациенты первой группы дополнительно получали метформин, второй группы – инсулинотерапию инсулином НПХ на ночь. При проведении сравнительной оценки эффективности и переносимости терапии констатировано одинаковое улучшение показателей гликемии в группах сравнения, однако уровень холестерина сыворотки значительно снизился при приеме метформина (p<0,005), но не на фоне инсулинотерапии. Все пациенты инсулинотерапии предпочитали дополнительное назначение метформина.
Возможность использования Глюкованса сопровождается не только оптимизацией метаболического контроля, но и значимым улучшением приверженности к лечению по сравнению с использованием свободной комбинации составляющих этого препарата (рис. 8) [20].
Для выбора лечения и приверженности к нему важна и стоимость препарата. С экономической точки зрения применение комбинированного препарата Глюкованс – более выгодный вариант лечения СД 2 типа по сравнению с совместным применением препаратов метформина и гликлазида.
В настоящее время доступны другие комбинированные антигипергликемические препараты. Комбинации с тиазолидиндионами не получили широкого использования в связи с компрометирующими этот класс препаратов данными, свидетельствующими о повышении выраженности отеков, риска остеопороза, рака мочевого пузыря. Весьма перспективное направление современной диабетологии – фиксированная комбинация метформина и ингибиторов дипептидил-пептидазы-4. Преимущества такой комбинации: воздействие на сравнительно новый фактор патогенеза СД 2 – дефект инкретинов, эффективное снижение гликемии, очень низкий риск гипогликемических эпизодов, отсутствие прибавки массы тела, цитопротективное действие на бета-клетки. К сожалению, существенно ограничивает возможности использования комбинации метформина и ингибиторов дипептидил-пептидазы-4 ее стоимость, превышающая стоимость фиксированной комбинации метформина и глибекламида на 90% (по данным www.tabletka.by).
Таким образом, комбинированные препараты имеют ряд преимуществ. За счет более низких терапевтических доз комбинируемых препаратов они лучше переносятся, вызывают меньшее количество побочных эффектов, чем при монотерапии или при раздельном назначении комбинируемых лекарственных средств. При приеме комбинированных препаратов отмечается более высокая комплаентность, поскольку уменьшается количество и кратность приема таблеток. Комбинированные препараты позволяют назначать трехкомпонентную терапию.
Глюкованс обеспечивает возможность воздействия на два патогенетических дефекта одной таблеткой, препарат хорошо переносится и сравнительно дешев, оптимизирует «compliance» и «concordance» при длительном лечении и улучшает показатели долгосрочной компенсации СД 2. Однако строго фиксированная доза комбинированных препаратов вызывает и ряд трудностей при необходимости изменения дозы только одной составляющей. Наличие различных дозировок препаратов, входящих в состав комбинированного препарата (как для препарата Глюкованс), делает возможным более гибкий подбор именно оптимального, нужного соотношения комбинируемых препаратов. Глюкованс – единственный комбинированный препарат, имеющий в составе микронизированную форму глибенкламида, что позволяет снизить риск гипогликемии. Этот препарат составлен с учетом сбалансированной комбинации доз метформина 500 мг и глибенкламида 2,5 и 5 мг в одной таблетке, что предоставляет возможность выбора дозировок и возможность титрации доз.
Глюкованс имеет обширную доказательную базу – свыше 200 публикаций в различных странах мира. Суммируя эти данные, можно констатировать, что Глюкованс может быть препаратом первого выбора при поздней диагностике диабета. В качестве препарата второго выбора Глюкованс может быть использован при неэффективности максимальных доз препарата первого выбора, у пациентов с сохраненной секрецией инсулина при вторичной резистентности к препаратам сульфонилмочевины, при наличии противопоказаний к максимальным дозам метформина для проведения монотерапии.
*На правах рекламы. Статья впервые была опубликована в журнале «Ars Medica». – 2012. – №15(70). – С. 116– 125
Л И Т Е Р А Т У Р А
1. Махлина Е.С., Мохорт Т.В. // Актуальные проблемы медицины: м-лы Республ. науч.-практ. конф. и 19-й итоговой науч. сессии Гомельского гос. мед. ун-та, Гомель, 23–24 февраля 2010 г. – Гомель, 2010. – С.118.
2. Русаленко М.Г. // Журн. Гродн. гос. мед. ун-та. – 2008. – №4. – С.60–62.
3. Adherence to long-term therapy, evidence of action, 2003, www.who.int
4. Angelico F., Burattin M., Alessandri C. et al. // Cochrane Database Syst. Rev. – 2007. – Vol. (1). – CD005166.
5. Blonde L., Joyal S., Henry D., Howlett H. // Int. J. Clin. Pract. – 2004. – Vol.58 (9). – P.820–826.
6. Blonde L., Wogen J., Kreilick C., Seymour A.A. // Diabetes Obes. Metab. – 2003. – Vol.5 (6). – P.424–431.
7. Charpentier G., Fleury F., Kabir M. et al. // Diabet. Med. – 2001. – Vol.16. – P.828–834.
8. Chapman R.H., Benner J.S., Petrilla A.A. et al. // Arch. Intern. Med. – 2005. 23. – Vol. 165(10). – P.1147–1152.
9. Cho Y.M., Kieffer T.J. // Diabetologia. – 2011. – Vol.54 (2). – P.219–122.
10. Dailey G.E. // Expert. Opin. Pharmacother. – 2003. – Vol.4 (8). – P.1417–1430 (ISSN: 1465–6566).
11. Dailey G., Kim M.S., Lian J.F. // J. Int. Med. Res. – 2002. – Vol.30 (1). – P.71–79.
12. Dailey G., Kim M.S., Lian J.F. // Clin. Ther. – 2001. – Vol.23 (8). – P.1311–1120.
13. Davidson J.A., Scheen A.J., Howlett H.C. // Drug. Saf. – 2004. – Vol.27 (15). – P.1205–1216.
14. DeFronzo R.A. // Ann. Intern. Med. – 1999. – Vol.131. – P.281–303.
15. Donahue S.R., Turner K.C., Patel S. // Clin. Pharmacokinet. – 2002. – Vol.41. – P.1301–1309.
16. Garber A.J., Bruce S., Fiedorek F.T. // Clin. Ther. – 2002. – Vol.24. – P.1401–1413.
17. Gastadelli A. et al. // Diabetologia. – 2004. – Vol.47. – P.31–39.
18. Hoerger T.J., Segel J.E., Gregg E.W., Saaddine J.B. // Diabetes Care. – 2008. – Vol.31 (1). – P.81–86.
19. Kocak M., Caliskan E., Simsir C., Haberal A. // Fertil. Steril. – 2002. – Vol.77. – P.101–106.
20. Melikian C., White T.J., Vanderplas A. et al. // Clin. Ther. –2002. – Vol.24 (3). – P.460–467.
21. Moses R., Carter J., Slobodniuk R. et al. // Diabetes Care. – 1999. – Vol.22. – P.119–124.
22. Trischitta V., Italia S., Raimondo M., Guardabasso V. et al. // J. Endocrinol. Invest. – 1998. – Vol.21 (11). – P.744–747.
23. Turner R.C ., Cull C.A., Frighi V., Holman R.R. // JAMA. – 1999. – Vol.281 (21). – P.2005–2012.
24. Vandermolen D.T., Ratts V.S., Evans W.S. et al. // Fertil. Steril. – 2001. – Vol.75. – P.669–673.
Медицинские новости. – 2013. – №11. – С. 57-61.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.