Внимание! Статья адресована врачам-специалистам
MokhortT.V.
Belarusian State Medical University
A rational choice of antihypergycemic therapy
in the practice of internist
Резюме. С учетом распространенности и роста заболеваемости сахарным диабетом (СД) 2-го типа определена целесообразность понимания принципов лечения заболевания интернистами. Обоснованы принципы определения гликемических целей при лечении СД 2-го типа. С позиций доказательной медицины обоснована последовательность в выборе антигипергликемических препаратов, используемых в лечении СД 2-го типа, включая модификацию образа жизни и метформин на первом этапе. Интенсификация терапии базируется на альтернативном выборе препаратов сульфонилмочевины, тиазолидиндионов, инкретин-ассоциированной терапии и ингибиторов натриевого котранспортера глюкозы. Проведен анализ эффективности и безопасности гипогликемизирующих средств, используемых до начала инсулинотерапии.
Ключевые слова: сахарный диабет 2-го типа, принципы лечения, антигипергликемическая терапия.
Медицинские новости. – 2018. – №3. – С. 49–55.
Summary. According the prevalence and growth of the incidence of type 2 diabetes mellitus (DM 2), the expediency of understanding the principles of treating the disease by internists is determined. The principles of glycemic goals the determination in the treatment of diabetes have been substantiated. On the basis of evidence-based medicine, a sequence in the selection of antihyperglycemic drugs used in the treatment of DM 2, including a modification of the lifestyle and metformin at the first step, is justified. The intensification of therapy is based on an alternative choice of sulfonylurea preparations, thiazolidinediones, incretin-associated therapy and inhibitors of sodium glucose cotransporter. The effectiveness and safety of hypoglycemic agents used before the onset of insulin therapy was analyzed.
Keywords: type 2 diabetes mellitus, principles of glycemic goals, antihypergycemic therapy.
Meditsinskie novosti. – 2018. – N3. – P. 49–55.
В 2017 году в мире зарегистрировано 425 млн пациентов с сахарным диабетом (СД), при этом более 90% составляют пациенты с СД 2-го типа. Нарастающая распространенность заболевания привела к тому, что в большинстве развитых стран мира эта патология является предметом наблюдения врачей общей практики и/или терапевтов. Кроме того, пациент с СД 2-го типа, как правило, имеет коморбидную патологию (избыточную массу тела или ожирение, артериальную гипертензию, дислипидемию, неалкогольную жировую болезнь печени и др.), нуждающуюся в лечении интерниста и определяющую увеличение риска смертности. Основной причиной смерти при СД 2-го типа является кардиоваскулярная патология, что диктует необходимость анализа выбора антигипергликемической терапии с позиций влияния на кардиоваскулярные риски.
Цели антигипергликемической терапии в настоящее время определяются необходимостью увеличения продолжительности и качества жизни, что направлено на профилактику рисков смерти от сердечно-сосудистой патологии и предупреждение микрососудистых осложнений (ретинопатия, невропатия, нефропатия). Именно поэтому краеугольным камнем в выборе тактики лечения является определение целевых уровней компенсации по уровню гликированного гемоглобина (НbА1с) и гликемии, которые обеспечивают предупреждение смертности и инвалидизации.
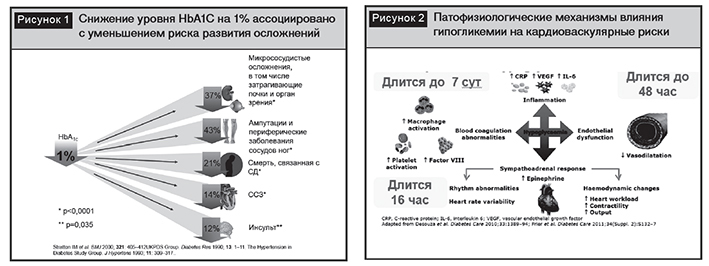
На протяжении длительного времени, с момента окончания классического исследования UKPDS (UnitedKingdomProspectiveDiabetesStudy), бытовала точка зрения, основанная на необходимости достижения и поддержания длительной нормогликемии, обеспечивающей снижение риска развития микро- и макрососудистых осложнений у пациентов с впервые выявленным СД 2-го типа (рис. 1) [24]. Однако позднее было неопровержимо доказано, что достижение показателей НbА1с менее 6,5% ассоциировано с увеличением риска кардиоваскулярной смертности вследствие развития гипогликемических эпизодов [23]. Патофизиологические механизмы, реализующиеся при гипогликемии, включают активацию симпатоадреналового ответа с увеличением частоты сердечных сокращений, вариабельностью сердечного ритма и другими гемодинамическими нарушениями, развитие эндотелиальной дисфункции с нарушением вазодилатации, стимуляцию образования провоспалительных и прокоагуляционных факторов (рис. 2), действие которых не ограничивается временем купирования гипогликемии, а продолжается до нескольких суток [9, 10]. Кроме того, гипогликемия является фактором, обусловливающим развитие постгипогликемических гипергликемий, ограничивая возможность достижения компенсации, возникновение когнитивных нарушений, повышение риска травматизма.
Перечисленные факторы привели к пониманию необходимости дифференцированного подхода к выбору целей контроля гликемии в зависимости от ряда факторов (рис. 3). Доказано, что достижение уровня НbА1с<7% ассоциировано со снижением риска развития микро- и макроангиопатий и смертности, поэтому именно этот показатель определен в качестве целевого для подавляющего большинства пациентов с СД 2-го типа (табл. 1) [2]. Более строгий контроль (<6,5%) может быть рекомендован пациентам с небольшим стажем СД, длительной ожидаемой продолжительностью жизни, при лечении препаратами, обеспечивающими низкий риск возникновения гипогликемических эпизодов и при отсутствии сердечно-сосудистой патологии. Менее строгий контроль (<8%) является допустимым у пациентов с тяжелыми и повторяющимися гипогликемиями, с небольшой ожидаемой продолжительностью жизни, наличием декомпенсированных сердечно-сосудистых заболеваний или микроангиопатий, при наличии тяжелых сопутствующих осложнений или длительном течении СД, когда тяжело достичь целевых значений гликемии [12].

Таблица 1. Целевые уровни компенсации сахарного диабета 2-го типа
|
НbА1с<6,5%
|
НbА1с<7,0%
|
НbА1с<8,0–8,5%
|
|
небольшой стаж СД
длительная ожидаемая
продолжительность жизни
лечение препаратами,
обеспечивающими низкий риск
гипогликемических эпизодов
отсутствие сердечно-сосудистой
патологии
|
для подавляющего
большинства
пациентов
|
тяжелые,
повторяющиеся
гипогликемии
небольшая ожидаемая
продолжительность жизни
наличие декомпенсиро-
ванных сердечно-
сосудистых заболеваний
или микроангиопатий
длительное течение СД,
когда тяжело достичь
целевых значений гликемии
|
Дополнительным фактором, лимитирующим лечение СД 2-го типа, является наличие избыточной массы тела и потенциальное ее увеличение при использовании некоторых антигипергликемических агентов.
Все перечисленные факторы определяют понимание того факта, что при выборе тактики антигипергликемической терапии следует основываться на обеспечении снижения гликемии без гипогликемических эпизодов и набора массы тела. Для удобства использования и при отсутствии необходимости частого исследования НbА1с (согласно Национальным протоколам лечения СД 2-го типа данное исследование рекомендуется проводить 2 раза в год) в таблице 2 приведены соотношения уровней НbА1с и среднесуточного уровня гликемии.
Таблица 2. Соотношение НbА1с и уровней среднесуточной гликемии
|
НbА1С (%)
|
Средний
уровень глюкозы крови (mmol /L)
|
|
4
5
6
7
8
9
10
11
12
|
2,6
4,5
6,7
8,3
10,0
11,6
13,3
15,0
16,7
|
Существует множество различных национальных протоколов и рекомендаций по выбору тактики лечения СД 2-го типа, которые основаны на использовании единого принципа: начальный этап лечения включает рекомендации по коррекции образа жизни, направленного на нормализацию массы тела за счет изменения питания и увеличения физических нагрузок.
Далее рекомендуются различные алгоритмы интенсификации лечения. Наиболее рациональным является алгоритм, основанный на дифференциации тактики в зависимости от исходной степени декомпенсации, то есть от уровня НbА1с. Новые рекомендации опубликованы экспертами Американской диабетологической ассоциации в 2018 г. Дифференцированный поход к антигипергликемической терапии включает в себя ранее опубликованные рекомендации Американского колледжа эндокринологов и Российские клинические рекомендации «Алгоритмы специализированной медицинской помощи больным сахарным диабетом». Этот подход не противоречит национальным протоколам лечения СД 2-го типа [1] и рекомендует:
– пациентам с НbА1с менее 9% использование монотерапии, которая включает коррекцию образа жизни и назначение метформина;
– пациентам с НbА1с около 9% – «двойную» терапию (с добавлением второго антигипергликемического агента);
– пациентам с НbА1с более 9–10% – «тройную» терапию, включающую добавление третьего антигипергликемического препарата, включая начало инсулинотерапии.
Первые 2 этапа являются прерогативой врача-интерниста, поэтому рассмот-рим подробно особенности лечения СД 2-го типа на этих этапах.
В настоящее время указывается на необходимость одновременного соблюдения рекомендаций по коррекции образа жизни, обучению в «Школе диабета» и назначения метформина. Это обусловлено низкой эффективностью коррекции образа жизни на популяционном уровне в связи с игнорированием рекомендаций и результатами исследования LookAHEAD, продемонстрировавшего отсутствие снижения риска смертности от кардиоваскулярных событий в когорте интенсивной коррекции образа жизни [25]. Основные механизмы действия метформина связаны с влиянием на чувствительность к инсулину и представлены на рисунке 4.
Выбор метформина в качестве препарата первой линии обусловлен целым рядом известных фактов:
· доказанная эффективность и безопасность в течение 60 лет и более;
· крайне низкий риск развития гипогликемических эпизодов;
· отсутствие прибавки массы тела;
· доказательство снижения смертности от инфаркта миокарда, инсульта, госпитализаций по причине хронической сердечной недостаточности;
· снижение риска развития рака [5].
В настоящее время доказаны плейо-тропные влияния метформина, включающие способность снижать риск развития СД 2-го типа у пациентов с предиабетом, уменьшать проявления кардиоваскулярных рисков при СД 1-го типа, оптимизировать овуляцию и фертильность при синдроме поликистозных яичников, оказывать позитивное влияние на состояние кишечной микробиоты, улучшать когнитивную функцию, оказывать влияние на плод у женщин с гестационным диабетом, являясь потенциалом для долгосрочных «программных» воздействий на плод по снижению риска развития последующего ожирения [5].
Использование метформина ограничивается только наличием противопоказаний или непереносимости, то есть данное лекарственное средство является «базисным» препаратом в лечении СД 2-го типа. Рекомендуемая начальная доза метформина составляет 500 мг в день с последующей ее медленной титрацией до 3000 мг в сутки, что минимизирует появление побочных эффектов в виде диспепсии.
Наиболее значимые побочные эффекты метформина: нарушение вкуса, снижение аппетита, тошнота/рвота, боли в животе или диарея, которые минимизируются при медленной титрации дозы. Около 5% пациентов имеют непереносимость метформина. Следует помнить, что данное лекарственное средство противопоказано при снижении скорости клубочковой фильтрации (СКФ) менее 30 мл/мин/1,73 м2 и не рекомендуется инициировать лечение при СКФ 30–45 мл/мин/1,73 м2 или оценить риск и пользу при потенциальном начале лечения (степень гипергликемии, риск гипогликемии, возрастающий при снижении СКФ). Рекомендуется отменять метформин перед рентгеноконтрастными исследованиями при СКФ 30–60 мл/мин/1,73 м2 в связи с риском развития лактат-ацидоза (крайне редкое, но тяжелое осложнение использования метформина).
В случае, если компенсация не достигнута в течение 3 месяцев, рекомендуется либо ужесточение рекомендации по коррекции образа жизни (при отсутствии редукции массы тела), либо переход к «двойной» терапии. Потенциальные варианты выбора наиболее используемых антигипергликемических препаратов второго выбора приведены в таблице 3.
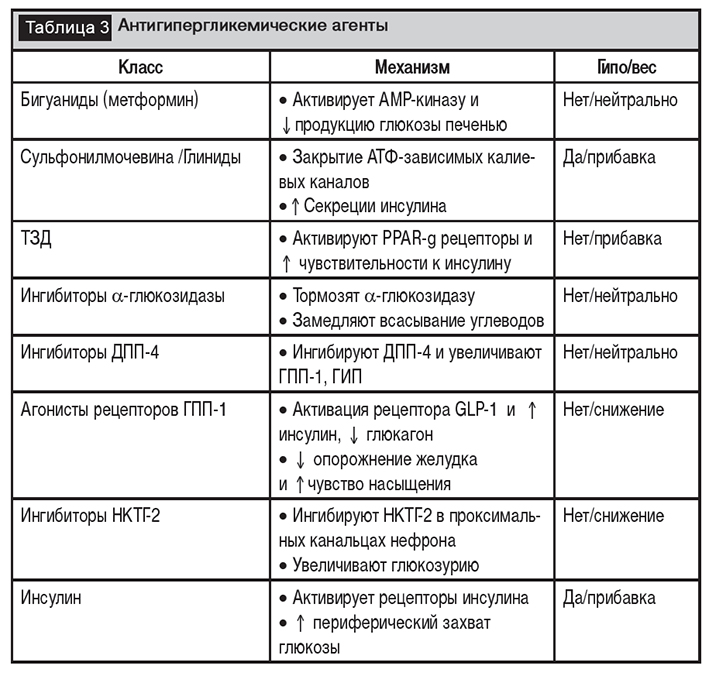
На протяжении многих лет актуальным остается бета-центрический подход к лечению СД 2-го типа, обусловленный доказанными прогрессирующими нарушениями пульсирующего характера секреции и первой фазы секреции инсулина, увеличением доли проинсулина, нечувствительностью бета-клеток к гипергликемии при развитии заболевания.Поэтому препаратами выбора являются секретагоги инсулина, в частности, производные сульфонилмочевины (ПСМ), что отражено в национальных протоколах лечения СД 2-го типа [1]. Доказано, что при течении СД 2-го типа происходит постепенная потеря функции бета-клеток поджелудочной железы в среднем на 4% в год, поэтому через несколько лет от начала заболевания многие пациенты нуждаются в использовании ПСМ или препаратов инсулина. ПСМ усиливают секрецию инсулина за счет стимуляции бета-клеток поджелудочной железы, способствуют восстановлению их чувствительности к гипергликемии, увеличивают число инсулиновых рецепторов.
Обладая одинаковым механизмом антигипергликемического действия, ПСМ имеют различия в степени селективности относительно взаимодействия молекулы со специфическими рецепторами (SUR – sulfonylureareceptor) на АТФ-зависимых калиевых каналах, расположенных в плазматической мембране бета-клеток. SUR экспрессированы не только на бета-клетках поджелудочной железы, но и в волокнах скелетных мышц, гладкомышечных клетках, нейронах головного мозга, кардиомиоцитах. При этом в различных тканях изоформы рецепторов варьируют: например, в бета-клетках выявлена изоформа SUR1, в поперечнополосатых мышечных волокнах и миокарде – SUR2A, в гладкомышечных клетках – SUR2B, в нейронах головного мозга и гладкомышечных клетках сосудов – SUR2A и 2B. Блокада SUR в кардиомиоцитах и гладкомышечных клетках сосудистой стенки небезопасна, так как может приводить к усилению ишемии миокарда, что имеет принципиальное значение для пациентов с кардиальной патологией. Очевидно, что повышение селективности ПСМ (соотношение влияния на АТФ-зависимые калиевые каналы бета-клеток поджелудочной железы и на те же каналы в других тканях) определяет их безопасность. Селективность различных ПСМ неодинакова (рис. 5), что объясняет различия в профиле кардиоваскулярной безопасности ПСМ.
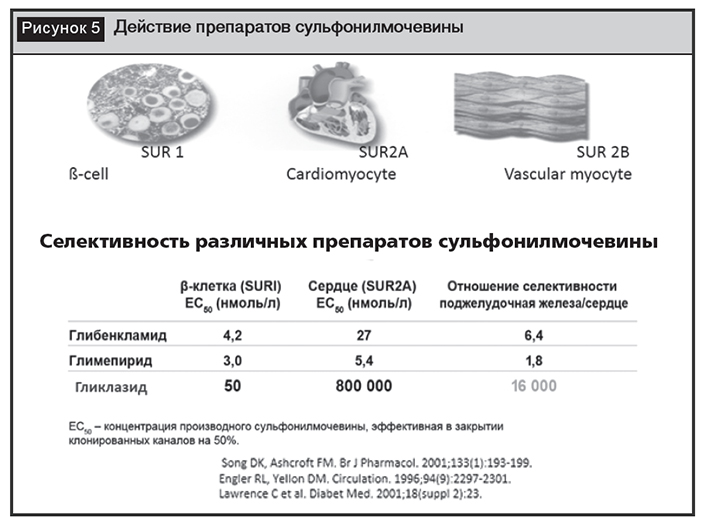
В национальных протоколах [1] указано, что из препаратов ПСМ могут быть назначены глибенкламид, гликлазид или гликвидон. В настоящее время клиницисты отдают предпочтение гликлазиду, так как в крупнейшем исследовании ADVANCE (ActioninDiabetesandVascularDisease: PreteraxandDiamicronMRControlledEvaluation), проведенном на пациентах высокого риска сердечно-сосудистой патологии, было доказано, что при безопасно контролируемом уровне глюкозы в крови до среднего уровня HbA1c 6,5%, отмечено уменьшение на 10% общего риска развития серьезных осложнений диабета и достигнута положительная тенденция к снижению риска сердечно-сосудистой смерти.
Анализ французского регистра, проведенный М. Zeller и соавт. по сравнению смертности от инфаркта миокарда при использовании различных ПСМ, показал, что прием глибенкламида ассоциируется с практически трехкратным увеличением риска смерти по сравнению с таковым при применении гликлазида и глимепирида [28].
Результаты согласуются с данными исследования ADVANCE, в котором было продемонстрировано, что использование гликлазида приводило к снижению уровня HbA1c на 1%, уменьшению риска развития микроваскулярных событий на 26% и макроваскулярных осложнений – на 22%, общей смертности – на 22%, а сердечно-сосудистой смертности – на 25% [19]. Эти результаты принципиально отличаются от данных других крупных исследований (ACCORD, VADT с использованием других антигипергликемических средств), в которых использовали другие ПСМ (глибенкламид, глимепирид) и тиазолидиндионы [23]. В качестве факторов, которые обеспечивают снижение кардиоваскулярных рисков при использовании гликлазида, доказано влияние низкого риска гипогликемий и минимизация прибавки массы тела при приеме гликлазида. Кроме того, гликлазид обладает уникальными антиоксидантными свойствами, включая уменьшение количества свободных радикалов, способствуя защите ?-клеток от апоптоза, замедляет окисление липопротеидов низкой плотности, угнетает выработку провоспалительных цитокинов, что в итоге обеспечивает вазодилатацию и опосредованно защищает от развития микроангиопатий и атеросклероза [8, 15, 20].
Приведенные выше результаты получены при использовании оригинальной молекулы гликлазида, известной на региональном рынке под названием «Диабетон МВ». История этого препарата насчитывает более 40 лет использования с доказанными эффектами, подтверждающими эффективность и безопасность терапии.
Тем не менее, Всемирная организация здравоохранения сохраняет в списке основных лекарств глибенкламид, что обусловлено его распространенностью и низкой стоимостью, а также важно для обеспечения доступности гипогликемизирующей терапии.
При недостижении целевых уровней HbA1c может быть начата «тройная» терапия с использованием различных антигипергликемических препаратов, включая инсулинотерапию.
Альтернативные варианты антигипергликемической терапии включают потенциальное использование тиазолидиндионов, ингибиторов альфа-глюкозидаз кишечника, глинидов, или регуляторов прандиальной гликемии, инкретин-ассоциированных препаратов, ингибиторов натриевого котранспортера глюкозы 2.
Тиазолидиндионы (ТЗД) – высокоселективные активаторы рецепторов пролифераторов пероксисом типа гамма. Они изменяют транскрипцию генов, принимающих участие в метаболизме углеводов и жиров, увеличивают чувствительность к инсулину, утилизацию глюкозы и снижение ее синтеза, преимущественно, в жировой и мышечной ткани. В настоящее время доступно использование пиоглитазона, который наряду с позитивными эффектами (уменьшение выраженности ИР, эффективное снижение гликемии с низким риском гипогликемий, откладывание инициации инсулинотерапии, позитивным влиянием на липидный спектр, уменьшением выраженности висцерального ожирения, микроальбуминурии, сосудистых молекул адгезии, С-реактивного белка, повышением уровня адипонектина, возможностью комбинировать с другими антигипергликемическими средствами) сопряжено с повышением массы тела, риском переломов, задержкой жидкости, в том числе при сердечной недостаточности, увеличением активности печеночных ферментов и вероятным повышением риска развития рака мочевого пузыря. Использование пиоглитазона сопровож-дается уменьшением частоты смерти от всех причин, нефатального инфаркта миокарда и инсульта [7], увеличением частоты развития сердечной недостаточности [11].
Ингибиторы всасывания глюкозы (акарбоза, воглибоза) оказывают гипогликемический эффект за счет замедления расщепления полисахаридов и всасывания моносахаридов в кишечнике различными глюкозидазами. Основной побочный эффект – активизация процессов брожения, поэтому продолжительное лечение сопровождается изменением кишечной микробиоты, микробной ферментацией углеводов со снижением рН фекальных масс, что может быть потенциальным фактором риска развития рака кишечника и сопровождаться диспептическими нарушениями. Препараты этой группы редко рекомендуются для монотерапии СД 2-го типа, но могут использоваться в комплексной терапии для потенцирования антигипергликемического эффекта или при манифестации СД 2-го типа.
Глиниды – регуляторы прандиальной гликемии (натеглинид и репаглинид) являются альтернативой инсулиновых секретагогов, поэтому их прием ассоциирован с риском возникновения гипогликемических эпизодов, увеличения массы тела, как и ПСМ, что лимитировало проведение рандомизированных исследований с их использованием и широкое распространение. Согласно последним рекомендациям, этот класс препаратов может быть рекомендован при аллергических реакциях при применении препаратов сульфонилмочевины и/или невозможности регулярного приема пищи.
Современными препаратами являются лекарственные средства, действие которых обусловлено влиянием на уровне инкретинов – гормонов, вырабатывающихся в кишечнике. Препараты этого класса реализуют эффект на уровне коррекции дефекта секреции инкретинов – глюкагонподобного пептида 1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП), которые являются регуляторами гомеостаза глюкозы, оказывая многофакторное влияние.
· Стимуляция секреции инсулина в ответ на пищевую нагрузку (в отличие от других секретагогов, стимулирующих выработку инсулина в соответствии с фармакокинетикой).
· Ингибиция продукции глюкагона, секреция которого повышена при СД 2-го типа.
· Уменьшение продукции глюкозы печенью.
· Замедление процесса всасывания в кишечнике.
· Снижение аппетита.
Кроме того, описаны их плейотропные эффекты, включающие замедление апоптоза бета-клеток, активацию их пролиферации, системные антиоксидантные влияния, результирующиеся в нейро-, нефро-, кардио- и гепатопротективные эффекты.
В клинической практике используются в качестве препаратов инкретин-ассоциированного действия:
· агонисты или миметики ГПП-1 (АГПП-1: эксенатид, лираглутид, ликсисенатид, дулаглютид и др.), вызывающие эффекты ГПП-1 в супрафизиологических концентрациях;
· ингибиторы дипептидилпептидазы-4 (ИДПП-4) – фермента, лимитирующего действие эндогенных инкретинов, вызывая их деградацию через несколько минут после их секреции (ситаглиптин, вилдаглиптин, линаглиптин, саксаглиптин, алоглиптин и др.), и способствующих сохранению физиологических концентраций ГПП-1 и ГИП за счет ингибиции эндогенной деградации нативных инкретинов.
Доказано, что препараты этого класса обеспечивают снижение уровня гликемии и HbA1c без гипогликемических эпизодов, не вызывая прибавки массы тела, а АГПП-1 вызывают значимое снижение массы тела. Перечисленные бенефиции позволяли ожидать не только обеспечения компенсации, но и снижения кардиоваскулярных рисков, что получило подтверждение в ряде исследований, проведенных у пациентов с высоким кардиальным риском.
ИДПП-4 в течение 3 лет не оказывают негативного влияния на риски развития кардиальных событий, но не обеспечивают его снижения [10, 21, 27] (рис. 6). Обсуждается вопрос о частоте госпитализаций по причине сердечной недостаточности при использовании ИДПП-4, так как опубликованы спорные факты. Однако одно из последних наблюдений за когортой 1 499 650 пациентов с СД 2-го типа в реальной клинической практике продемонстрировало, что уровень госпитализаций не ассоциирован с использованием инкретин-ассоциированной терапии по сравнению с другими оральными антидиабетическими средствами у пациентов без анамнеза сердечной недостаточности [14, 22].
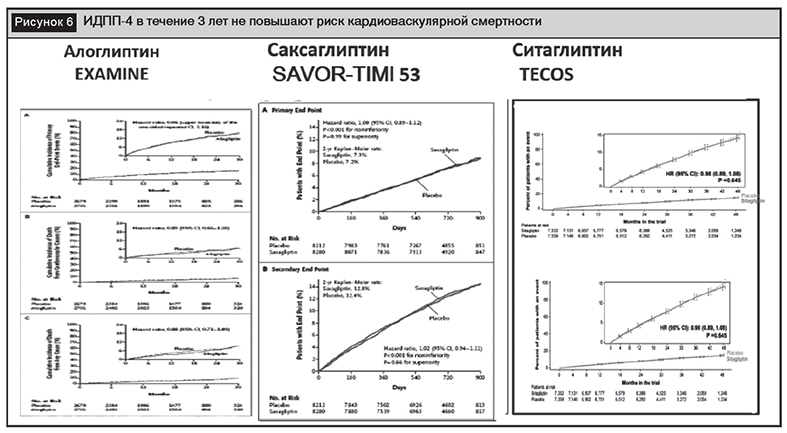
При выборе ИДПП-4 следует понимать, что они способны обеспечить снижение HbA1c на 0,5–0,7%, поэтому их назначение целесообразно при возможности обеспечения достижения целевых уровней компенсации. Преимущества этого класса препаратов включают: отсутствие прибавки массы тела, крайне низкий риск гипогликемий, возможности использования у пожилых пациентов, при снижении скорости клубочковой фильтрации, вплоть до терминальных стадий ХБП, при печеночной недостаточности, то есть в тех клинических ситуациях, когда риск возникновения гипогликемических эпизодов повышается.
Альтернативным вариантом могут быть АГПП-1, которые являются инъекционными лекарственными средствами. Несмотря на парентеральный путь введения, АГПП-1 имеют преимущества, которые основываются на отсутствии необходимости коррекции режима питания (что необходимо при инициации инсулинотерапии), низком риске развития гипогликемий, снижении, массы тела в среднем на 8 кг, возможности комбинаций с другими антигипергликемическими препаратами. В отличие от ИДПП-4, АГПП-1 продемонстрировали снижение риска развития сердечно-сосудистых событий в когорте пациентов высокого риска, что дает им еще одно важное преимущество [16, 17].
Для улучшения комплаентности к настоящему времени созданы и доступны комбинированные препараты ИДПП-4 с метформином (и в Республике Беларусь) и АГПП-1 с аналогами инсулина.
Последний класс антигипергликемических препаратов селективных ингибиторов натриевого котранспортера глюкозы 2 (ИНКГ-2) – глифлозинов, представленных эмпаглифлозином, канаглифлозином, даптоглифлозином и др., оказывает действие на уровне почечных канальцев, повышая реабсорбцию глюкозы. Глифлозины ингибируют работу натрий-глюкозных котранспортеров, что приводит к значимому уменьшению реабсорбции глюкозы за счет блокады обратного захвата глюкозы в проксимальных канальцах нефронов в S1-сегменте проксимальных канальцев почек и увеличению выделения глюкозы с мочой [3, 13].
Антигипергликемический эффект глифлозинов не зависит от секреции или активности инсулина, а определяется увеличенной потерей глюкозы с мочой. Препараты обеспечивают снижение HbA1c, массы тела при отсутствии гипогликемических эпизодов. Кроме того, доказано, что при применении ИНКГ-2 регистрируется снижение артериального давления вследствие осмодиуреза, повышение чувствительности тканей к инсулину и улучшение функции бета-клеток в эксперименте и индекса ИР (НОМА) у лиц с СД 2-го типа. Побочные эффекты глифлозинов обусловлены увеличением глюкозурии и потенциальным повышением риска развития урогенитальных инфекций.
К настоящему времени опубликованы результаты рандомизированных многоцентровых исследований EMPA-REG OUTCOME и CANVAS по использованию эмпаглифлозина и канаглифлозина, продемонстрировавшие в когортах пациентов высокого кардиального риска снижение смертности от сердечно-сосудистых заболеваний, нефатального инфаркта или нефатального инсульта, госпитализаций по причине сердечной недостаточности [18, 29]. В ходе динамического наблюдения за пациентами установлено, что различия в показателях отмечаются уже через 3 месяца от начала лечения, что свидетельствуют о том, что не только снижение гликемии, артериального давления и массы тела определяют результат, на основании чего предложены различные гипотезы, объясняющие прямое кардиопротективное влияние ИНКГ-2. Несмотря на то, что нарушение функции почек с СКФ менее 45 мл/мин/1,73 м2, доказано, что ИНКГ-2 оказывают ренопротективный эффект, который проявляется снижением макро- и микроальбуминурии и сохранением скорости клубочковой фильтрации, уменьшением скорости снижения расчетного показателя СКФ [26].
В настоящее время глифлозины привлекают внимание клиницистов, так как продемонстрированные эффекты превосходят позитивные влияния метформина, ТЗД, ПСМ и ИДПП-4, что позволяет рекомендовать их широкое использование при выборе второго или третьего антигипергликемического препарата и использование в виде монотерапии при наличии ограничений в использовании метформина. В то же время, кроме риска возникновения урогенитальных инфекций, опубликованы данные по повышению риска развития нормогликемического кетоацидоза, особенно при СД 1-го типа, повышения риска низкотравматичных переломов и ампутаций при использовании канаглифлозина, не зарегистрированного в Республике Беларусь. Также важно понимать, что препараты этого класса (ИНКГ-2) увеличивают глюкозурию, что может приводить к повышению риска развития урогенитальных инфекций и предопределяет необходимость отбора комплаентных пациентов и контроля общего анализа мочи при первичном назначении препарата.
Выбор второго и/или третьего антигипергликемического препарата может быть основан на потребности использования льготного назначения (глибенкламид, гликлазид, гликвидон), при наличии сопутствующей патологии, лимитации в использовании различных классов антигипергликемических препаратов, а также с учетом мотивации врача и пациента.
При выборе двойной терапии следует учитывать, что в настоящее время обосновано последовательное использование новых опций в лечении СД 2-го типа. В исследовании CVD-REAL NORDIC при использовании ИНКГ-2 было связано с уменьшением риска сердечно-сосудистой смертности, крупными неблагоприятными сердечно-сосудистыми событиями и госпитализации по причине сердечной недостаточности. В субгруппе по оценке эффективности ИНКГ-2, в основном дапаглифлозина, при проведении анализа кардиоваскулярных исходов было определено, что максимальное снижение рисков наблюдалось у пациентов, получавших до инициации терапии ИНКГ-2 препараты ПСМ [4].
Последним этапом в лечении СД 2-го является инсулинотерапия, назначение которой является прерогативой эндокринолога, требует дополнительных навыков и знаний и не рассматривается в данной публикации. Дополнительной опцией при сочетании ожирения и декомпенсации называется использование метаболической хирургии, обеспечивающей снижение массы тела, улучшение компенсации углеводного обмена и увеличение продолжительности жизни.
В завершение необходимо подчерк-нуть, что при первом контакте с пациентом с СД 2-го типа, следует предупредить его о неизбежности инсулинотерапии при длительном течении заболевания. При этом время инициации инсулинотерапии может быть отложено, если пациент добивается целевых показателей гликемии, для чего необходимо его активное участие в лечении – соблюдение рекомендаций по здоровому образу жизни с редукцией массы тела.
Л И Т Е Р А Т У Р А
1. Приказ Министерства здравоохранения Республики Беларусь от 02.07.2013 №764 «Об утверждении клинических протоколов диагностики и лечения взрослого населения с заболеваниями эндокринной системы при оказании медицинской помощи в амбулаторных условиях».
2. American Diabetes Association 6. // Diabetes Care. – 2018. – Vol.41 (Suppl. 1). – S55–S64.
3. Bailey C.J.// Trends Pharmacol Sci. – 2011. – Vol.32, N2. – P.63–71.
4. Birkeland K.I., Jørgensen M.E., Carstensen B., et al. // Lancet Diabetes Endocrinol. – 2017. – Vol.5, N9. – P.709–717.
5. Clifford J. // Diabetologia. – 2017. – Vol.60. – P.1566–1576.
6. Desouza C.V., Bolli G.B., Fonseca V. // Diabetes Care. – 2010. – Vol.33, N6. – P.1389–1394.
7. Dormandy J.A., Charbonnel B., Eckland D.J., et al. // Lancet. – 2005. – Vol.366. – P.1279–1289.
8. Fava D., Cassone-Faldetta M., Laurenti O., et al. // Diabetologia 48. – P.1541–1548.
9. Frier B.M., Schernthaner G., Heller S.R. // Diabetes Care. – 2011. – Vol.34 (Suppl. 2). – S132–S137.
10. Green J.B., Bethel M.A., Armstrong P.W., et al. // NEJM. – 2015. – Vol.373. – P.232–242.
11. Hernandez A.V., Usmani A., Rajamanickam A., Moheet A. // Am. J. Cardiovasc. Drugs. – 2011. – Vol.11, N2. – P.115–128.
12. International Hypoglycaemia Study Group.http://care.diabetesjournals.org/content/38/8/1583. // Diabetes Care. – 2015. – Vol.38, N8. – P.1583–1591.
13. Kalra S. // Diabetes Ther. – 2014. – Vol.5, N2. – P.355–366.
14. Kristian B. // NEJM. – 2016. – Vol.374. – P.1145–1154.
15. Lortz S., Gurgul-Convey E., Lenzen S., Tiedge M. // Diabet. Med. – 2002. – Vol.19, N9. – P.752–757.
16. Marso S.P., Daniels G.H., Brown-Frandsen K., et al. // NEJM. – 2016. – Vol.375. – P.311–322.
17. Marso S.P., Bain S.C., Consoli A., et al. // NEJM. – 2016. – Vol.375, N19. – P.1834–1844.
18. Neal B., Perkovic V., Mahaffey K.W., et al. // NEJM. – 2017. – Vol.377. – P.644–657.
19. Patel A., MacMahon S., Chalmers J., et al. // NEJM. – 2008. – Vol.358. – P.2560–2572.
20. Sawada F., Inoguchi T., Tsubouchi H., et al. // Metabolism. – 2008. – Vol.57. – P.1038–1045.
21. Scirica B.M., Bhatt D.L., Braunwald E., et al. // NEJM. – 2013. – Vol.369, N14. – P.1317–1326.
22. Secrest M.H., Udell J.A., Filion K.B. // Trends Cardiovasc. Med. – 2017. – Vol.27, N3. – P.194–202.
23. Skyler J.S., Bergenstal R., Bonow R.O., et al. // J. Am. Coll. Cardiol. – 2009. – Vol.53, N3. – P.298–304.
24. Stratton I.M., Adler A.I., Neil H.A., et al. // BMJ. – 2000. – Vol.321, N7258. – P.405–412.
25. The Look AHEAD Research Group Cardiovascular Effects of Intensive Lifestyle Intervention in Type 2 Diabetes // NEJM. – 2013. – Vol.369. – P.145–154.
26. Wanner C., Inzucchi S.E., Lachin J.M., et al. // NEJM. – 2016. – Vol.375, N4. – P.323–334.
27. White W.B., Cannon C.P., Heller S.R., et al. // NEJM. – 2013. – Vol.369, N14. – P.1327–1335.
28. Zeller M., Danchin N., Simon D., et al. // JCEM. – 2010. – Vol.95, N11. – P.4993–5002.
29. Zinman B., Wanner C., Lachin J.M., et al. // NEJM. – 2015. – Vol.373. – P.2117–2128.
Медицинские новости. – 2018. – №3. – С. 49-55.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.