Внимание! Статья адресована врачам-специалистам
Seliun Yu.A.1, Valentsiukevich A.V.2, Kolyadko M.G.2, Ostrovsky Yu.P.2
1«Republican Clinical Medical Centre» of the Presidential Administration of the Republic of Belarus, Minsk
2Republican Scientific and Practical Center «Cardiology», Minsk, Belarus
Deficiency of antithrombin III activity and its correction in a cardiosurgical patient
Резюме. Рассмотрен клинический случай профилактики развития тромбоза у пациента с системой экстракорпоральной мембранной оксигенации, находящегося на лечении в Республиканском научно-практическом центре «Кардиология». Представлены преимущества использования концентрата антитромбина III перед свежезамороженной плазмой и высокими дозами гепарина. Описаны механизмы развития гепаринорезистентности и ее коррекция.
Ключевые слова: экстракорпоральная мембранная оксигенация, концентрат антитромбина III, атенатив.
Медицинские новости. – 2018. – №4. – С. 46–50.
Summary. This article was demonstrated a clinical case of prevention of thrombosis of an oxygenator in a patient with an extracorporeal membrane oxygenation system being treated in the Republican Scientific and Practical Center «Cardiology». The advantages of antithrombin III concentrate compare to fresh frozen plasma and high doses of heparin were described. The mechanisms of heparin resistance development and its correction are described.
Keywords: extracorporeal membrane oxygenation, antithrombin III concentrate, atenativ.
Meditsinskie novosti. – 2018. – N4. – P. 46–50.
Одной из важнейших задач в лечении кардиохирургического пациента является профилактика развития тромбоза при проведении экстракорпоральных процедур, таких как искусственное кровообращение (ИК), экстракорпоральная мембранная оксигенация (ЭКМО), внутриаортальная баллонная контрпульсация (ВАБК), заместительная почечная терапия (ЗПТ) и др.
После открытия гепарина McLean в 1916 году и его антидота, протамина, гепарин эффективно используют в качестве основного метода антикоагуляции в кардиохирургии [1].
В 1966 году P.G. Hattersley [2] ввел показатель «активированное время свертывания крови» (АВСК) для мониторинга антикоагулянтного эффекта гепарина. Когда АВСК не достигает целевых уровней после введения гепарина, возникает опасение, что антикоагуляция является недостаточной. Это может приводить к образованию тромбов в контуре ИК, на поверхности системы ВАБК, в оксигенаторе ЭКМО, в контуре ЗПТ или в организме пациента.
Клинический случай
Пациент Б., 58 лет, 70 кг, 27.07.2017 года госпитализирован в кардиохирургическое отделение Республиканского научно-практического центра «Кардиология» с диагнозом: «Ишемическая болезнь сердца: атеросклеротический кардиосклероз. Недостаточность митрального клапана с регургитацией на клапане IV степени. Отрыв хорды митрального клапана. Недостаточность трикуспидального клапана с регургитацией на клапане III степени. HIIa, NYHAII. Двусторонний гидроторакс».
03.08.2017 года пациенту была выполнена операция «Протезирование митрального клапана из миниторакотомного доступа», которая проводилась на фоне однолегочной вентиляции. Операция осложнилась острым повреждением правого легкого (рис. 1), что потребовало подключения периферической вено-артериальной системы ЭКМО.
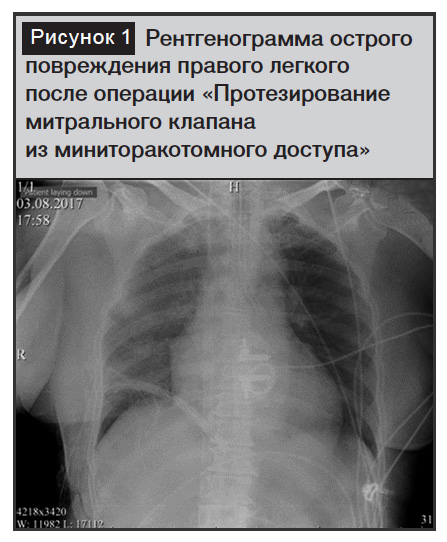
При исследовании системы гемостаза за 3 дня до операции по данным коагулограммы была нормокоагуляция (табл. 1).
Таблица 1. Показатели коагулограммы до операции
|
Показатели
коагулограммы
|
Значение
|
|
АЧТВ
|
25,0 с
|
|
ПВ
|
15,8 с
|
|
МНО
|
1,16
|
|
ТВ
|
18,0 с
|
|
Фибриноген
|
5,0 г/л
|
|
АТ III
|
108%
|
|
АВСК
|
116 с
|
ИК проведено по стандартной методике нормотермической перфузии (36 °С). Расчетная доза гепарина перед началом ИК составила 27 500 МЕ болюсом и 5000 МЕ в первичное заполнение физиологического контура ИК. После введения гепарина АВСК составило 514 с. В период проведения ИК для поддержания целевого АВСК (более 480 с) потребовалась дополнительная доза гепарина 7500 МЕ. Время ИК составило 286 минут.
После подключения системы ЭКМО и поступления в отделение кардиохирургической реанимации АВСК определяли каждые 2–4–6 часов. Целевое АВСК поддерживалось в диапазоне значений 180–220 с. Для этого через 6 часов после операции было назначено постоянное внутривенное введение нефракционированного гепарина (НФГ) в дозе 400 МЕ в час. Через 14 часов после операции, на фоне повышения доз гепарина до 700 МЕ в час, уровень АВСК составил 146 с. Активность АТ III в сыворотке крови составила 59%. Для профилактики развития тромбоза в оксигенаторе ЭКМО и снижения рисков возникновения кровотечения на фоне повышения доз НФГ было введено 2000 МЕ концентрата АТ III. АВСК увеличилось до 204 с. Уровень активности АТ III составил 87%. Доза гепарина была уменьшена до 500 МЕ в час. На этом фоне количество отделяемого по дренажам не возросло: за 1-е сутки – 400 мл, за 2-е – 400 мл, за 3-и – 180 мл. Концентрат АТ III в дозе 2000 МЕ вводился трижды при снижении АТ III менее 70% (табл. 2).
Таблица 2. Динамика АВСК, дозы вводимого гепарина и уровня АТ III в первые 36 часов после операции
|
Показатель
|
АВСК,
с
|
Гепарин доза, МЕ/ч
|
АТ III,
%
|
|
Поступление в КХР
|
128
|
–
|
66
|
|
Через 6 часов после операции
|
142
|
400
|
60
|
|
Через 14 часов после операции
|
146
|
700
|
59
|
|
После одного введения 2000 МЕ концентрата АТ III
|
204
|
500
|
87
|
|
Через 24 часа после операции
|
135
|
800
|
58
|
|
После второго введения 2000 МЕ концентрата АТ III
|
213
|
500
|
85
|
|
Через 36 часов после операции
|
154
|
900
|
62
|
|
После третьего введения 2000 МЕ концентрата АТ III
|
198
|
600
|
91
|
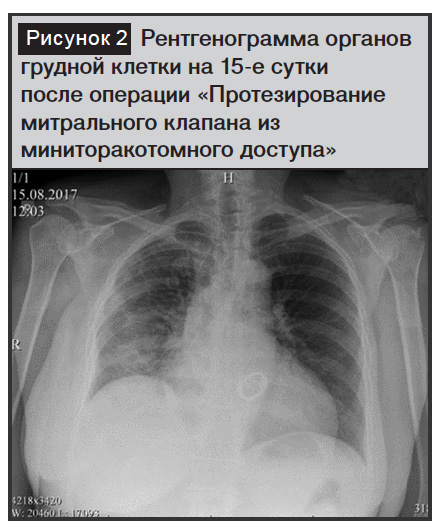
Через 5 суток после операции и отключения системы ЭКМО пациенту назначен варфарин. На 7-е сутки после стабилизации состояния и достижения целевого МНО (2,5–3,5) пациент переведен из отделения кардиохирургической реанимации в отделение кардиохирургии. На 15-е сутки выписан из стационара с улучшением клинической картины (рис. 2).
Обсуждение
Гепаринорезистентность при проведении ИК определяется как недостаточность необычно высоких доз гепарина для достижения целевого АВСК. По данным литературы, частота возникновения резистентности к гепарину при кардиохирургических вмешательствах составляет от 4 до 26% [3, 4]. При профилактике тромбозов гепаринорезистентность ряд авторов определяют как невозможность достичь целевого уровня антикоагуляции при использовании 35 000 МЕ гепарина в сутки [5]. Этот вопрос менее изучен.
НФГ представляет собой гетерогенную смесь полисахаридов с молекулярным весом от 5000 до 30 000 Да (5–35 единиц полисахарида) со средней молекулярной массой 15 000 Да [6].
Гепарин является естественным соединением бычьего либо свиного происхождения. Первичный механизм действия гепарина косвенно опосредуется запуском антикоагулянтного эффекта АТ III, эндогенного ингибитора тромбина (фактор IIa), фактора Ха и других факторов. Вторичный механизм действия включает катализирующие антикоагулянтные свойства кофактора II гепарина (ГК II).
НФГ – антикоагулянт выбора при проведении вспомогательных методик кровообращения, поскольку он эффективен, недорог и легко инактивируется. Однако основным недостатком НФГ является его вариабельный антикоагулянтный эффект среди пациентов. Множество факторов способствует этой вариабельности.
Вариабельность чувствительности к гепарину среди пациентов имеет биохимическую и фармакокинетическую основу. Биохимическое связывание гепарина и АТ III зависит от гепарина, обладающего критической пентасахаридной последовательностью, которая присутствует только в одной трети молекул гепарина [7]. Молекулы гепарина, не имеющие этой критической последовательности, могут обладать различной антикоагулянтной активностью, а также вносить вклад в ряд других неблагоприятных эффектов [8]. Кроме того, длина цепи гепарина должна содержать не менее 18 сахаридов для образования тройного комплекса «гепарин – AT III – тромбин» и действовать в качестве матрицы, с которой могут взаимодействовать как АТ III, так и тромбин [9]. Когда этот комплекс образуется, ингибирование тромбина ускоряется в 4000 раз [10]. Однако фибринсвязанный тромбин защищен от комплекса «гепарин – АТ III» и не ингибируется [11]. В то же время, ингибирование фактора Ха путем АТ III может происходить при длине цепи <18 сахаридов и требует только, чтобы гепарин содержал определенную последовательность пентасахаридов. Ингибирование фактора Ха ускоряется в 1200 раз [10].
Лабораторно уровень AT III может быть измерен как тестом активности (то есть функциональный анализ), так и тестом уровня антигена [12]. Оба теста обычно выражаются в процентах с нормальными значениями от 80 до 120%. Функциональный анализ измеряет способность АТ III ингибировать тромбин или фактор Ха в присутствии гепарина. Количество тромбина или фактора Xa, остающегося свободным, обратно пропорционально уровню AT III [12]. Уровень антигена определяет только количество АТ III в крови. Из двух тестов функциональный анализ является наиболее подходящим, поскольку он обнаруживает как количественные, так и качественные дефекты в АТ, в то время как уровень антигена определяет только количественные дефекты.
Дефицит АТ III считается одним из основных механизмов устойчивости к гепарину, поскольку антикоагуляционный эффект гепарина опосредован через АТ III-путь. Таким образом, дефицит АТ III уменьшает способность гепарина ингибировать тромбин.
По этиологии различают врожденный и приобретенный дефицит АТ III. Врожденный дефицит АТ III имеет место у 1 из 3000 человек, и у этих пациентов уровень АТ III – приблизительно 40–60% от нормального [13].
Приобретенный дефицит АТ III связан с различными клиническими состояниями, включая заболевания печени, недоедание, нефротический синдром, а также лечение гепарином [14].
Доказано, что использование НФГ за 24–48 часов до операции способствует развитию гепаринорезистентности [15]. Это же наблюдается и при использовании такого НМГ, как эноксапарин [16]. При введении гепарина комплекс «гепарин – АТ III» связывается с тромбином и следует за распадом гепарина из комплекса «тромбин – АТ III». Затем комплекс «тромбин – АТ III» быстро потребляется и выводится с помощью ретикулоэндотелиальной системы, что приводит к снижению уровня АТ III примерно на 5–7% в день [17]. Это уменьшение уровня АТ III является механизмом, благодаря которому дооперационное применение гепарина увеличивает частоту резистентности к гепарину [18]. M.D. Linden и соавт. продемонстрировали более низкие уровни АТ III в предоперационном периоде (80,9% против 92,6% активности) [18].
Существуют и другие причины приобретенного дефицита АТ III. Сниженный синтез может наблюдаться у пациентов с заболеваниями печени (например, циррозом) и недостаточным питанием [19]. Заболевание почек может привести к постоянной потере АТ III с мочой [20]. Нарушение системы гемостаза, наблюдаемое при сепсисе, диссеминированном внутрисосудистом свертывании и у пациентов с тромбозом глубоких вен/тромбоэмболией легочной артерии, может приводить к более высокому потреб-лению АТ III [21]. Наблюдается снижение уровня АТ III у пациентов с механическими поддерживающими устройствами работы сердца (ВАБК, ЭКМО, обходы желудочков сердца) [22, 23].
Совместно с АТ III-зависимыми механизмами гепаринорезистентности существуют и АТ III-независимые механизмы, которые могут привести к устойчивости к гепарину. R.C. Becker и соавт. [24] при-шли к выводу, что внутривенный нитроглицерин привел к качественному дефекту АТ III, M.J. Brack и соавт. [25] наблюдали снижение дозы гепарина при одновременной инфузии с нитроглицерином. Независимо от потенциального механизма, влияние внутривенного введения нитроглицерина на чувствительность гепарина остается неопределенным, что продемонстрировано в нескольких исследованиях, дающих противоречивые результаты [26–28].
Когда врач встречается в клинической практике с картиной гепаринорезистентности, его лечебная тактика включает:
1. введение дополнительных доз гепарина;
2. добавление AT III при помощи трансфузии свежезамороженной плазмой (СЗП);
3. добавление концентрата AT III.
Как правило, дополнительная доза гепарина вводится до тех пор, пока АВСК не достигнет целевых уровней. Увеличение дозы гепарина для достижения целевого АВСК может привести к нежелательным последствиям, поскольку общая доза гепарина коррелирует со степенью эффекта «рикошета» гепарина и потенциальным риском возникновения кровотечения [29]. J.H. Levy и соавт. [30] продемонстрировали, что концентрация гепарина в цельной крови >4 единиц/мл не привели к дальнейшему увеличению AВСК. Кроме того, высокие дозы гепарина требуют введения высоких доз протамина для нейтрализации, что увеличивает риск возникновения побочных эффектов протамина [31]. Высокие дозы гепарина также связывают с повышенным риском развития гепарин-индуцированной тромбоцитопении [32]. Подбор эффективной дозы гепарина связан с дополнительными затратами времени, что нежелательно в экстренных ситуациях [33].
Еще одним нежелательным аспектом использования повышенных доз гепарина является усиление потребления АТ III, что может быть связано с нежелательными последствиями в послеоперационном периоде. В рандомизированном исследовании M. Ranucci и соавт. [34] сравнивалось использование повышенных доз гепарина с концентратом АТ III для преодоления гепаринорезистентности при проведении ИК. Было показано, что применение повышенных доз гепарина связано со снижением уровня АТ III в послеоперационном периоде. В то же время ряд исследований показал, что дефицит АТ III в послеоперационном периоде связан с различными тяжелыми осложнениями, включая фатальные; увеличением сроков госпитализации и затрат здравоохранения [35–37]. Вопрос коррекции дефицита АТ III в послеоперационном периоде мало изучен: в детской кардиохирургии положительный опыт в профилактике тромбозов получен с помощью оценки уровня АТ III и возмещении AT при использовании концентрата при уровне АТ менее 50% [38]. Вопрос ведения концентрата АТ в послеоперационном периоде у взрослых решался с позиций гепаринорезистетности [5]. Все изложенное позволяет сделать вывод, что в послеоперационном периоде следует обращать особое внимание на пациентов, которым при проведении ИК требовались повышенные дозы гепарина (выше 400 МЕ/кг по M. Ranucci), а также в случае длительности ИК более 2,5 часов, что связывают с повышенным риском развития тромботических осложнений [39]. Таким образом, использование в раннем послеоперационном периоде различных процедур, связанных с проведением ИК (ЭКМО, ЗПТ и др.), увеличивает вероятность дальнейшего снижения уровня АТ III. То же самое можно сказать о реоперациях с применением ИК.
В своей клинической практике мы используем следующий протокол.
1. Во время операций с использованием ИК. Перед началом проведения ИК, если у пациента не достигается целевое АВСК (более 400 с) на введение 400 МЕ/кг гепарина, после двух дополнительных болюсов гепарина 50–100 МЕ/кг вводим 500–1000 МЕ концентрата АТ III (Атенатив®).
2. Во время проведения интенсивной терапии уровень АТ III определяем не менее двух раз в сутки пациентам с ВАБК, ЭКМО, обходами желудочков сердца; пациентам на продленной ЗПТ с НФГ; лицам с высоким риском развития тромбоза, находящимся на лечении НФГ или НМГ. При снижении уровня AT III менее 70%, вводим концентрат АТ III в дозе 1000–4000 МЕ/сут. Пациентам с сепсисом или инфекционным эндокардитом также определяем уровень АТ III и вводим концентрат АТ III в дозе 1000–4000 МЕ в сутки, если уровень AT III<50%.
Успешное лечение гепаринорезистентности с добавлением АТ III путем трансфузии СЗП было впервые описано A.H. Sabbagh и соавт. [40]. СЗП является приемлемым с медицинской точки зрения методом добавления AT III и содержит приблизительно 1 МЕ AT III на 1 мл СЗП [41]. Таким образом, 2 дозы СЗП (приблизительно 500 мл) содержат около 500 МЕ AT III. Однако публикаций, поддерживающих СЗП как эффективное средство для лечения устойчивости к гепарину, ограниченное количество, проведено только 1 исследование in vitro и опубликовано несколько клинических случаев [42, 43]. Кроме того, нет исследований, показывающих, что введение СЗП при гепаринорезистентности улучшает клинические результаты.
Эффективность концентрата антитромбина в преодолении гепаринорезистентности при проведении ИК продемонстрирована в рандомизированных исследованиях [3, 4, 33]. M.S. Avidan и соавт. [3, 4] также продемонстрировали, что 2 доз СЗП недостаточно для улучшения ответа на гепарин у большинства пациентов. Авторы считают, что необходимо около 2 литров СЗП для коррекции дефицита АТ III [4]. СЗП может улучшить результаты при введении гепарина у небольшого процента пациентов. Однако проблемы безопасности при гемотрансфузии и удлинение времени до трансфузии при размораживании СЗП делают эту терапию менее привлекательной [44]. При возникновении гепаринорезистентности интраоперационно в случае операции с проведением ИК необходимо немедленное восстановление надлежащего уровня антикоагуляции, и использование СЗП в этом случае фактически невозможно, так как это требует длительных временных затрат, а также недопустима перегрузка объемом кардиохирургического пациента. Кроме того, в последние годы появляются данные о том, что введение СЗП может быть связано с повышенным риском развития тромбозов [45–47]. Это может быть связано с тем, что для коррекции относительно селективного дефицита одного или нескольких факторов свертывания или их ингибиторов (включая АТ III) вводятся все факторы коагуляции, и их концентрация может достигнуть критического уровня.
Концентрат АТ III появился как один из методов лечения дефицита активности АТ III. Он доступен как в очищенной человеческой, так и в рекомбинантной формах. Оба препарата поставляются во флаконах в виде стерильного лиофилизированного порошка, а эффективность стандартизована в соответствии с международным стандартом Всемирной организации здравоохранения. Источником очищенного человеческого АТ III является плазма здоровых доноров, при производстве препарата проводится инактивация вирусов. Источником рекомбинантного АТ III являются козы генной инженерии. Таким образом, рекомбинантный АТ III противопоказан пациентам с известной гиперчувствительностью к белкам козьего молока. Хотя обе формы концентрата АТ III увеличивают уровень АТ III, различия в клинической фармакологии влияют на дозировку. Период полувыведения рекомбинантного AT III намного короче, чем очищенного человеческого (11,6 часа против 3,8 дня) и требует поддерживающей инфузии для поддержания нормальной активности АТ III в течение длительного периода времени. Рекомбинантный AT III имеет в 4 раза выше сродство к гепарину, но клинически этой разницы не видно [48].
Заключение
ЭКМО – это методика, обычное использование которой связано со многими сложностями. Антикоагуляция гепарином является лишь одним из важных аспектов ЭКМО. В данной статье представлен клинический случай, при котором коррекция дефицита активности АТ III входила в комплексное лечение пациента, а также являлась полноценным методом профилактики тромбоза в оксигенаторе системы ЭКМО. К сожалению, минимальное АВСК, необходимое для безопасного проведения экстракорпоральных процедур, не всегда можно достичь повышением доз НФГ из-за развития гепаринорезистентности. Введение концентрата АТ III является одним из методов лечения АТ III-зависимой гепаринорезистентности. Использование концентрата АТ позволяет добиться быстрого и предсказуемого эффекта без риска возникновения ряда осложнений в отличие от СЗП и дополнительных доз гепарина. Использование концентрата АТ III может быть необходимо для профилактики развития тромбозов в послеоперационном периоде в ситуациях высокого риска.
Л И Т Е Р А Т У Р А
1. WardropD., KeelingD. // Br. J. Haematol. – 2008. – Vol.141. – P.757–763.
2. Hattersley P.G. // JAMA. – 1966. – Vol.196. – P.436–440.
3. Avidan M.S., Levy J.H., Scholz J., et al. // Anesthesiology. – 2005. – Vol.102. – P.276–284.
4. Avidan M.S., Levy J.H., van Aken H., et al. // J. Thorac. Cardiovasc. Surg. – 2005. – Vol.130. – P.107–113.
5. Peltier S., Domrault C., Maupetit J.-C., et al. // J. Pharm. Clin. – 2005. – Vol.24, N2. – P.70–76.
6. Johnson E.A., Mulloy B. // Carbohydr. Res. – 1976. – Vol.51. – P.119–127.
7. Choay J., Petitou M., Lormeau J.C., Sinar P., Casu B., Gatti G. // Biochem. Biophys. Res. Commun. – 1983. – Vol.116. – P.492–499.
8. Kishimoto T.K., Viswanathan K., Ganguly T., et al. // N. Engl. J. Med. – 2008. – Vol.358. – P.2457–2467.
9. Bray B., Lane D.A., Freyssinet J.M., Pejler G., Lindahl U. // Biochem. J. – 1989. – Vol.262. – P.225–232.
10. Jordan R.E., Oosta G.M., Gardner W.T., Rosenberg R.D. // J. Biol. Chem. – 1980. – Vol.255. – P.10081–10090.
11. Weitz J.I., Hudoba M., Massel D., Maraganore J., Hirsh J. // J. Clin. Invest. – 1990. – Vol.86. – P.385–391.
12. Patnaik M.M., Moll S. // Haemophilia. – 2008. – Vol.14. – P.1229–1239.
13. Tait R.C., Walker I.D., Perry D.J., et al. // Transfusion. – 1998. – Vol.38. – P.481–498.
15. Chan T., Hwang N.C., Lim C.H. // Perfusion. – 2006. – Vol.21. – P.99–103.
16. Bar-Yosef S., Cozart H.B., Phillips-Bute B., Mathew J.P., Grocott H.P. // Can. J. Anaesth. – 2007. – Vol.54. – P.107–113.
17. Matthai W.H.Jr, Kurnik P.B., Groh W.C., Untere-ker W.J., Siegel J.E. // J. Am. Coll. Cardiol. – 1999. – Vol.33. – P.1248–1256.
18. Linden M.D., Schneider M., Baker S., Erber W.N. // J. Cardiothorac. Vasc. Anesth. – 2004. – Vol.18. – P.131–135.
19. Segal H., Cottam S., Potter D., Hunt B.J. // Hepatology. – 1997. – Vol.25. – P.683–688.
20. Chen T.Y., Huang C.C., Tsao C.J. // Am. J. Hematol. – 1993. – Vol.44. – P.276–279.
21. Na S., Shim J.K., Chun D.H., Kim D.H., Hong S.W., Kwak Y.L. // World J. Surg. – 2009. – Vol.33. – P.1862–1867.
22. Niebler R.A., Christensen M., Berens R., Wellner H., Mikhailov T., Tweddell J.S. // Artif. Organs. – 2011. – Vol.35. – P.1024–1028.
23. Stiller B., Lemmer J., Merkle F., et al. // Intensive Care Med. – 2004. – Vol.30. – P.1814–1820.
24. Becker R.C., Corrao J.M., Bovill E.G., et al. // Am. Heart J. – 1990. – Vol.119. – P.1254–1261.
25. Brack M.J., More R.S., Hubner P.J., Gershlick A.H. // Blood Coagul. Fibrinolysis. – 1993. – Vol.4. – P.183–186.
26. Gayoso J.M. // J. Extra Corpor. Technol. – 1999. – Vol.31. – P.184–190.
27. Gonzalez E.R., Jones H.D., Graham S., Elswick R.K. // Ann. Pharmacother. – 1992. – Vol.26. – P.1512–1514.
28. Berk S.I., Grunwald A., Pal S., Bodenheimer M.M. // Am. J. Cardiol. – 1993. – Vol.72. – P.393–396.
29. Gravlee G.P., Rogers A.T., Dudas L.M., et al. // Anesthesiology. – 1992. – Vol.76. – P.393–401.
30. Levy J.H., Montes F., Szlam F., Hillyer C.D. // Anes th. Analg. – 2000. – Vol.90. – P.1076–1079.
31. Cuenca J., Diz P., Sampedro F., et al. // J. Extra Corpor. Technol. – 2013. – Vol.45, N4. – P.235–241.
32. Sakr Y. // Critical. Care. – 2011. – Vol.15. – P.211.
33. Williams M.R., D’Ambra A.B., Beck A., et al. // Ann. Thorac. Surg. – 2000. – Vol.70. – P.873–877.
34. Ranucci M., Baryshnikova E., Crapelli G., et al. // J. Thorac. Cardiovasc. Surg. – 2013. – Vol.145. – P.1393–1399.
35. Ranucci M., Frigiola A., Menicanti L., et al. // Crit. Care Med. – 2005. – Vol.33. – P.355–360.
36. Garvin S., Muehlschlegel J.D., Perry T.E., et al. // Anesth. Analg. – 2010. – Vol.111. – P.862–869.
37. Muedra V., Llau J., Llagunes J., et al. // J. Cardiothorac. Vasc. Anesth. – 2013. – Vol.27, N2. – P.230–237.
38. Petäjä J., et al. // J. Thorac. Cardivasc. Surg. – 1999. – Vol.118, N5. – P.955–956.
39. Tanaka K., Esper S., Bolliger D. // Br. J. Anaesth. – 2013. – Vol.111 (Suppl.1). – i35–i49.
40. Sabbagh A.H., Chung G.K., Shuttleworth P., Applegate B.J., Gabrhel W. // Ann. Thorac. Surg. – 1984. – Vol.37. – P.466–468.
41. Mintz P.D., Blatt P.M., Kuhns W.J., Ro-berts H.R. // Transfusion. – 1979. – Vol.19. – P.597–598.
42. Heller E.L., Paul L. // J. Extra Corpor. Technol. – 2001. – Vol.33. – P.245–248.
43. Leong C.K., Ong B.C. // Ann. Acad. Med. Singap. – 1998. – Vol.27. – P.877–879.
44. Spiess B.D. // Ann. Thorac. Surg. – 2008. – Vol.85. – P.2153–2160.
45. Ghazi L., et al. // Thromb. Res. – 2015. – Vol.136, N6. – P.1204–1210.
46. Maruyama H., et al. // Acta Med. Okayama. – 2012. – Vol.66, N1. – P.61–66.
47. Magee G., et al. // J. Am. Coll. Surg. – 2014. – Vol.219, N4. – P.190.
48. Edmunds T., Van Patten S.M., Pollock J., et al. // Blood. – 1998. – Vol.91. – P.4561–4571.
Медицинские новости. – 2018. – №2. – С. 46-50.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушен