Внимание! Статья адресована врачам-специалистам
Sujayeva V.A.
Republican Scientific and Practical Centre “Cardiology”, Minsk, Belarus
Peculiarities of patients with different forms of chronic
ischemic heart disease in combination with arterial hypertension:
unsolved problems and ways to overcome them
Резюме. Представлен обзор современных литературных данных об особенностях развития, течения и лечения различных форм хронической ишемической болезни сердца (в том числе стабильной болезни коронарных артерий) в сочетании с артериальной гипертензией. Акцент сделан на использовании Престилола – новой фиксированной комбинации ингибитора ангиотензинпревращающего фермента периндоприла и высококардиоселективного b-адреноблокатора бисопролола. Рассмотрены механизмы двойной кардиопротекции, которая достигается при использовании указанной фиксированной комбинации лекарственных средств при сочетании стабильной болезни коронарных артерий и артериальной гипертензии.
Ключевые слова: хроническая ишемическая болезнь сердца, стабильная болезнь коронарных артерий, артериальная гипертензия, кардиопротекция, престилол, фиксированная комбинация, периндоприл, бисопролол.
Медицинские новости. – 2018. – №10. – С. 4–10.
Summary. The article gives an overview of modern literature data on the features of development, course and treatment of patients with different forms of chronic ischemic heart disease (including stable coronary artery disease) in combination with arterial hypertension. The emphasis is on the use of Prestilol – new fixed combination of an inhibitor of the angiotensin converting enzyme perindopril and a highly cardioselective beta-adrenoblocker of bisoprolol. The mechanisms of double cardioprotection, which is achieved when using this fixed combination of drugs in combination of stable coronary artery disease and hypertension, are considered.
Keywords: chronic ischemic heart disease, stable coronary artery disease, arterial hypertension, cardioprotection, prestilol, fixed combination, perindopril, bisoprolol.
Meditsinskie novosti. – 2018. – N10. – P. 4–10.
Артериальная гипертензия (АГ) наряду с курением, дислипидемией, нарушением углеводного обмена и ожирением относится к модифицируемым факторам риска развития сердечно-сосудистых заболеваний (ССЗ), распространенность которых приобрела характер пандемии. По данным Всемирной организации здравоохранения (ВОЗ), распространенность АГ среди лиц в возрасте старше 25 лет в 2013 году достигла 40% [24], то есть с 1990 года имел место прирост на 113% [10]. В США около 65 млн взрослых жителей имеют АГ [19]. Смертность от ССЗ, вызванных АГ, достигает 45% [24]. По данным мета-анализа 61 исследования, включавшего почти 1 млн взрослых пациентов США, установлено, что повышение систолического артериального давления (САД) на 20 мм рт. ст. (и/или диастолического артериального давления (ДАД) – на 10 мм рт. ст.) удваивает риск смерти от ССЗ [6].
Параллельно с ростом заболеваемости АГ наблюдается увеличение частоты развития одной из форм ССЗ – ишемической болезни сердца (ИБС), на долю которой приходится наибольший вклад в структуре смертности от болезней системы кровообращения (БСК). За 20 лет (с 1993 до 2013 года) распространенность ИБС возросла на 65% [21, 13], ежегодно от осложнений ИБС во всем мире умирают более 7 млн человек [23].
В то же время надежда на успех в борьбе с БСК и их осложнениями есть, так как известно, что более низкий уровень АД ассоциируется с более низким сердечно-сосудистым риском (ССР), а будущие неблагоприятные сердечно-сосудистые события могут быть предотвращены именно путем снижения АД [25].
О необходимости достижения «целевого» уровня АД говорят все кардиологические сообщества, разрабатываются лечебные и профилактические стратегии, учитывающие национальные, географические и экономические особенности. Однако достичь контроля АД удается лишь у небольшой части леченных пациентов. Сопутствующая АГ выявляется у 71–82% лиц с ИБС. При этом контроль АД при наличии сочетания ИБС и АГ еще более проблематичен: по данным исследования, включавшего данные 4646 пациентов, при лечении АГ у лиц без сопутствующих заболеваний эффективное снижение АД имело место у 65%, при наличии сочетания АГ и ИБС их доля составила лишь 50% [13, 21].
Развитие ИБС на фоне АГ существенно ограничивает возможности лекарственной терапии обоих состояний, недостаточно эффективный контроль АД усугубляет прогрессирование ИБС и развитие ее осложнений, то есть формируется «порочный круг». Таким образом, существует необходимость поиска путей воздействия на общие патофизиологические механизмы развития АГ и ИБС.
В 1991 г. V. Dzau и E. Braunwald предложена концепция «сердечно-сосудистого континуума», который представляет собой непрерывную цепь взаимосвязанных изменений, начиная от воздействия факторов риска через постепенное возникновение и прогрессирование ССЗ и вплоть до развития терминального поражения сердца и смертельного исхода [8].
Позднее был предложен термин «гипертонический каскад» сердечно-сосудистого континуума, в котором центральную роль играет собственно АГ и гипертоническое поражение сердца, приводящее в финале к развитию необратимых терминальных изменений, минуя сразу несколько этапов классического континуума (рис. 1) [1].
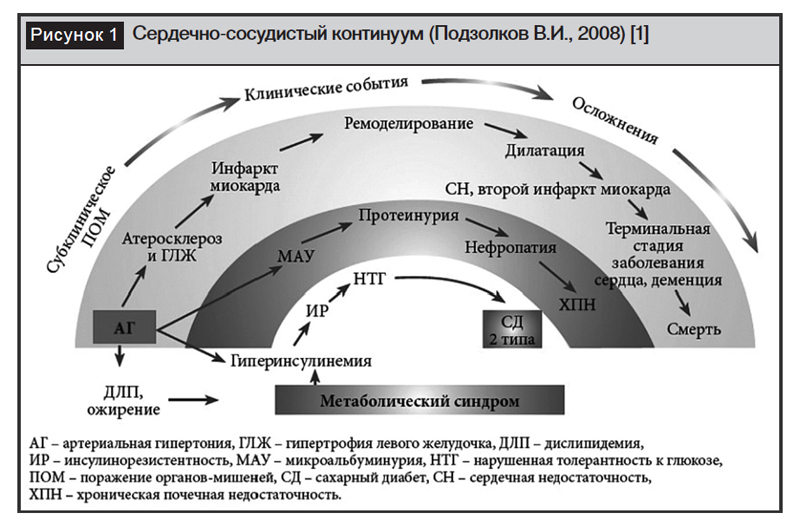
Непрерывная цепь взаимосвязанных изменений структуры и функции сразу нескольких органов и систем организма в рамках континуумапредполагает наличие общих патофизиологических процессов, механизмов развития и прогрессирования органных повреждений. В основном все многообразие подобных механизмов может быть сведено к генетическим, гемодинамическим и нейрогуморальным факторам. Одна из ведущих ролей принадлежит гиперактивации симпатоадреналовой системы (САС), которая является пусковым механизмом в цепочке каскада различных реакций при АГ и ИБС. Изначально некоторые из них носят приспособительный характер, при длительном существовании гиперсимпатикотонии происходит срыв компенсаторных механизмов и изначально приспособительные реакции приобретают патологический характер, причем, в процесс вовлекаются многочисленные органы и системы. Вазоконстрикторный эффект гиперсимпатикотонии реализуется в первую очередь через высвобождение нор-адреналина в синаптическую щель, далее норадреналин взаимодействует с адренорецепторами (АР) постсинаптической мембраны эффекторных клеток – гладкомышечных клеток сосудов. При АГ уменьшается количество постсинаптических АР и их чувствительность к стимуляции, что приводит к уменьшению вазодилатирующих и усилению вазоконстрикторных влияний катехоламинов.
Одновременно высокая активность САС стимулирует высвобождение ренина почками и запускает патологическую активацию ренин-ангиотензин-альдостероновой системы (РААС), что в совокупности приводит к росту общего периферического сопротивления сосудов (ОПСС), задержке натрия и воды и как результат – к дальнейшему повышению АД. Несмотря на то, что уровень норадреналина в плазме у лиц с АГ может не превышать нормальных показателей, инактивация его значительно замедляется, продлевая стимулирующие эффекты симпатической нервной системы на рецепторный аппарат органов-мишеней и сосудистую стенку, что проявляется в увеличении частоты сердечных сокращений (ЧСС) и ударного объема (УО), что способствует значительному повышению потребности миокарда в кислороде. При длительном существовании, а также при развитии атеросклероза в коронарных артериях это может приводить к формированию ишемии миокарда (рис. 2).
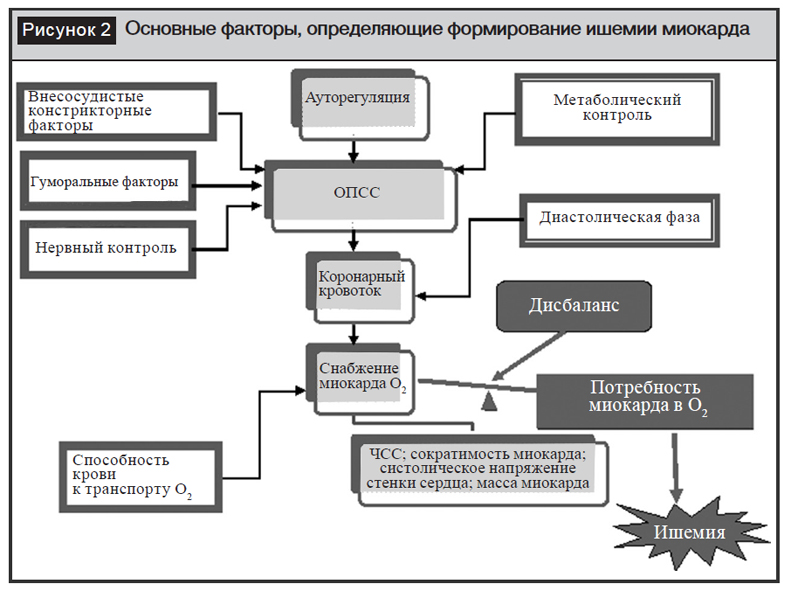
Рост ОПСС способствует повышению постнагрузки на миокард, что при длительном существовании приводит к развитию гипертрофии миокарда левого желудочка (ЛЖ). Последняя на начальных этапах носит компенсаторный характер и направлена на увеличение работы сердца и поддержание нормального сердечного выброса. В кардиомиоцитах увеличивается скорость репликации и дифференцировки ДНК, ускорение синтеза РНК и белка, индуцируется синтез миофибриллогена, новых саркомеров, митохондрий. Указанные изменения приводят к увеличению размеров кардиомиоцитов и повышению сократительной способности миокарда. По мере прогрессирования гипертрофии миокарда ЛЖ возникает несоответствие между возрастающей потребностью миокарда в кислороде и сниженными возможностями коронарного кровотока из-за сдавления инрамуральных ветвей коронарных артерий и прогрессирующим атеросклерозом. Развивается диффузная ишемия с последующей дистрофией и некротическими изменениями в кардиомиоцитах, в последствии они замещаются фиброзной тканью (см. рис. 2). Таким образом, адаптивная гипертрофия ЛЖ становится патологической (дезадаптивной), что и отражает дальнейшее продвижение по сердечно-сосудистому континууму от АГ к ИБС, ремоделированию миокарда и формированию сердечной недостаточности (СН). Повышенная активность САС способствует также развитию нарушений сердечного ритма вследствие электрической нестабильности миокарда, что в совокупности приводит к росту риска внезапной смерти.
К настоящему моменту получено достаточно доказательств того, что вмешательство в описанный «порочный круг» на любом этапе сердечно-сосудистого континуума способствует как уменьшению темпов прогрессирования и выраженности патологии сердечно-сосудистой системы, так и снижению риска развития осложнений и смерти.
Согласно Международной классификации болезней 10-го пересмотра (МКБ-10), выделяют основные формы хронической ИБС (рис. 3).
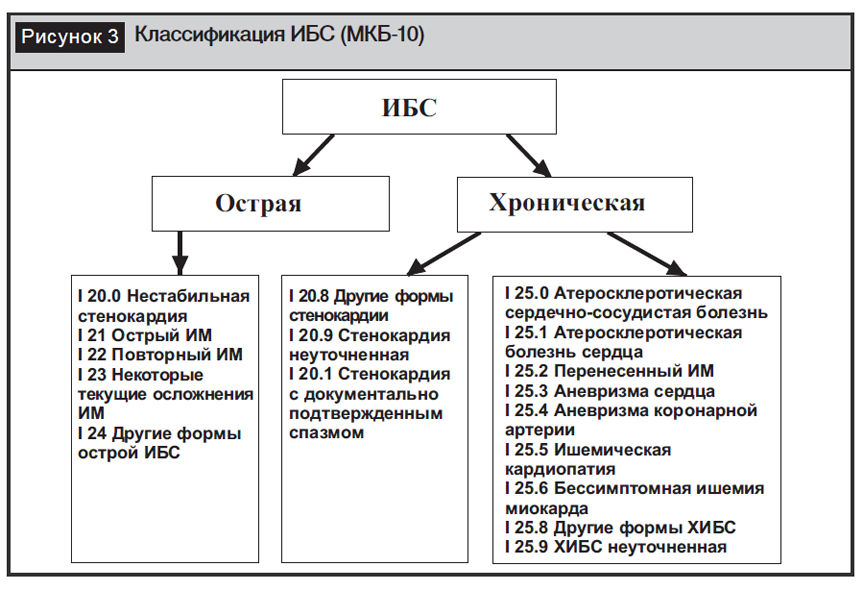
Учитывая особенности течения АГ в сочетании с различными формами ИБС, наличие общих механизмов развития, лечение этой категории пациентов представляет собой проблему, которая привлекла к себе внимание Американской ассоциации сердца/Американской коллегии кардиологов (АНА/АСС). В 2015 году был опубликован согласительный документ, рассматривающий проблему лечения пациентов с АГ и болезнью коронарных артерий (БКА), учитывающий полученные к настоящему моменту результаты крупных многоцентровых исследований [19].
В Рекомендациях АСС/АНА эксперты отмечают по-прежнему нерешенные вопросы лечения пациентов с АГ в сочетании с различными формами хронической ИБС (в том числе стабильной БКА) [19].
? Каким должен быть целевой уровень САД и ДАД у лиц с установленным диагнозом БКА?
? Является ли снижение уровня АД самим по себе защитным эффектом у лиц с БКА или имеют место какие-либо дополнительные протективные эффекты у отдельных классов антигипертензивных препаратов?
? Какие из антигипертензивных лекарственных средств особенно эффективны для проведения вторичной профилактики у лиц с ИБС?
? Какие антигипертензивные лекарственные средства должны использоваться у пациентов с установленным диагнозом стабильной БКА, какие – у лиц с острым коронарным синдромом (ОКС) – нестабильной стенокардией, инфарктом миокарда (ИМ) с и без подъема сегмента ST, а какие – в случае хронической сердечной недостаточности (ХСН), сформировавшейся вследствие ИБС?
При создании данного согласительного документа предпринята попытка суммировать все имеющиеся доказательства в отношении методов лечения и вторичной профилактики, наиболее эффективных у лиц, имеющих сочетание АГ и стабильной БКА. Сделан акцент на том, что у данной категории пациентов важно не только достижение снижения АД, но и положительное влияние на течение и исход имеющейся стабильной БКА.
Вопрос целевого уровня АД при наличии стабильной БКА в сочетании с АГ по-прежнему представляет собой предмет дискуссии, так как у этой категории пациентов одинаково неблагоприятным является наличие как высокого, так и чрезмерно низкого уровня АД – зависимость можно представить в виде J-кривой. При лечении стабильной БКА в сочетании с АГ дискутировался вопрос о целесообразности достижения определенного уровня пульсового АД, а также вопрос о необходимости дифференцированного подхода к коррекции САД и ДАД с учетом возраста, так как в разных возрастных группах уровень САД и ДАД имеет различное прогностическое значение [19].
По данным J.L. Izzo, A.H. Gradman [12], чрезмерное снижение ДАД может способствовать ухудшению коронарной перфузии, которая осуществляется именно в фазу диастолы. Коронарный кровоток имеет собственную ауторегуляторную систему. Уменьшение АД ниже ауторегуляторного порога может способствовать снижению перфузионного давления в коронарном русле и, как следствие, приводить к ухудшению перфузии миокарда. При исследованиях, проведенных у собак, было установлено, что использование ингибиторов ангиотензинпревращающего фермента (иАПФ) способствует восстановлению ауторегуляторного механизма и улучшению коронарной перфузии, что может являться патофизиологической основой эффективности иАПФ у лиц со стабильной БКА.
Еще одним из возможных механизмов положительного действия иАПФ у лиц со стабильной БКА в сочетании с АГ является возможность влиять на гипертрофию кардиомиоцитов и ремоделирование миокарда и сосудистой стенки, что способствует повышению резерва коронарного кровотока – способности к вазодилятации в условиях повышения потребности миокарда в кислороде и, как следствие – улучшению миокардиальной перфузии.
Весьма интересные данные о взаимосвязи АД с прогрессированием коронарного атеросклероза были получены в исследовании CAMELOT. По данным внутрисосудистого ультразвукового исследования (ВСУЗИ), было установлено, что снижение АД менее 120/80 мм рт. ст. способствовало уменьшению размера атеросклеротической бляшки на 4,6 мм3, при уровне АД 120–139/80–89 мм рт. ст. размер бляшки не менялся, а при АД ≥140/90 мм рт. ст. наблюдалось увеличение объема бляшки на 12 мм3 [20].
Цели лечения АГ у пациентов с хронической стабильной стенокардией:
– профилактика развития смерти, ИМ и инсульта;
– уменьшение частоты и длительности эпизодов ишемии миокарда;
– улучшение симптомов стенокардии.
Суммируя все данные, у лиц, имеющих сочетание АГ и различных форм ИБС, экспертами АСС/АНА (2015) рекомендовано достижение приведенных «целевых» уровней АД (табл. 1).
Таблица 1. Целевые уровни АД у лиц с различными форами ИБС (по AHA/ACC/ASH Scientific Statement, 2015) [19]
|
Артериальное давление
|
Нозологическая форма
|
Класс/
уровень доказанности
|
|
<140/90 мм рт. ст.
|
стабильная БКА
ОКС
ХСН
|
IIa/B
IIa/C
IIa/B
|
|
<130/80 мм рт. ст.
|
после перенесенного ИМ
|
IIb/B
|
!!! NBУ пациентов с АГ и стабильной БКА для вторичной профилактики неблагоприятных сердечно-сосудистых событий рекомендовано достижение целевого АД <140/90 мм рт. ст. (класс IIa, уровень доказанности В).
Более низкий целевой уровень АД рекомендовано достигать при лечении пациентов с АГ и стабильной БКА, перенесших ИМ, инсульт или транзиторную ишемическую атаку (ТИА), а также при наличии АГ в сочетании с клиническими эквивалентами высокого риска наличия стабильной БКА (болезнь каротидных артерий, периферических артерий, патологическая аневризма аорты) (класс IIb, уровень доказанности C).
У лиц, имеющих повышенное ДАД и стабильную БКА с доказанной ишемией миокарда, снижение АД и достижение его целевого уровня должно быть более медленным. При этом следует избегать снижения ДАД <60 мм рт. ст. у всех пациентов, имеющих сопутствующий сахарный диабет, и у лиц старше 60 лет. У пожилых пациентов с высоким пульсовым АД снижение САД может сопровождаться выраженным (<60 мм рт. ст.) снижением ДАД. Этого следует избегать, а при выявлении более тщательно обследовать на предмет обнаружения симптомов и признаков ишемии миокарда (класс IIa, уровень доказанности C).
В 2018 году Европейское общество кардиологов в очередной раз пересмотрело Рекомендации по лечению артериальной гипертензии. В зависимости от наличия коморбидной патологии при лечении АГ рекомендованы следующие «целевые» уровни САД/ДАД (табл. 2).
Таблица 2. Целевые значения офисного АД при лечении АГ в зависимости от наличия сопутствующих заболеваний
(2018 ESC/ESH Guidelines for the management of arterial hypertension Williams B., Mancia G., Spiering W. et al. European Heart Journal (2018) 00, 1–98)
|
Возрастная группа
|
АГ
|
+СД
|
+ХБП
|
+БКА
|
+инсульт /ТИА
|
ДАД
|
|
18–65 лет
|
130 или ниже при хорошей переносимости, но не ниже 120
|
130 или ниже при хорошей переносимости, но не ниже 120
|
<140 до 130 при хорошей переносимости
|
130 или ниже при хорошей переносимости, но не ниже 120
|
130 или ниже при хорошей переносимости, но не ниже 120
|
70–79
|
|
65–79 лет
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
70–79
|
|
≥80 лет
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
130–139 при хорошей переносимости
|
70–79
|
|
Целевое значение офисного ДАД, мм рт.ст.
|
70–79
|
70–79
|
70–79
|
70–79
|
70–79
|
|
Примечание: СД – сахарный диабет; ХБП – хроническая болезнь почек.
По мнению экспертов ESC (2018), начинать терапию АГ при наличии сопутствующей БКА у лиц в возрасте 18–79 лет необходимо при уровне САД ≥140 мм рт. ст., ДАД ≥90 мм рт. ст., у лиц в возрасте старше 80 лет – при АД ≥160/90 мм рт. ст. соответственно.
Еще один вопрос, требующий дальнейшего изучения, является выбор оптимального антигипертензивного лекарственного средства для инициации терапии АГ в сочетании с различными формами ИБС. Если для лечения АГ без сопутствующей патологии важен сам факт снижения АД, то в отношении сочетания АГ с ИБС эффективность различных классов антигипертензивных лекарственных средств для вторичной профилактики ССЗ и их осложнений существенно отличается.
По мнению экспертов АСС/АНА (2015) и ESC (2018), БАБ являются препаратами первой линии в лечении АГ в сочетании со стабильной БКА.
Их положительное воздействие на симптомы стенокардии и/или признаки ишемии миокарда у данной категории пациентов существенно превышают их отрицательный инотропный эффект. Уменьшение ЧСС увеличивает диастолу и, как следствие, способствует улучшению коронарной перфузии. Кроме того, БАБ уменьшают освобождение ренина из юкстагломерулярного аппарата. Рекомендовано отдавать предпочтения высококардиоселективным (?1) агентам [19], к которым относится бисопролол.
С учетом результатов недавно проведенных исследований высказывались сомнения относительно использования БАБ в качестве препаратов первой линии для лечения АГ при отсутствии сопутствующих заболеваний, однако, у пациентов, перенесших ИМ и/или имеющих симптомы/признаки ХСН, их приоритетность неоспорима. Для длительной базисной терапии БАБ также рекомендовано рассматривать в качестве препаратов первой линии у всех пациентов, имеющих коронарную и/или сосудистую патологию.
!!!NB1. БАБ рекомендовано использовать в качестве препаратов первой линии для лечения АГ в сочетании со стабильной БКА, перенесших ИМ и/или имеющих ХСН/систолическую дисфункцию (ФВ ≤40%) для уменьшения симптомов стенокардии/признаков ишемии миокарда у указанной категории пациентов (класс I, уровень доказанности В).
2. Длительность приема БАБ – не менее 3 лет у всех пациентов с нормальной функцией ЛЖ после перенесенного ИМ или ОКС (класс I, уровень доказанности В) [19].
Рекомендации АСС/АНА по эффективности различных лекарственных средств для лечения ИБС в сочетании с АГ с учетом принципов медицины, основанной на доказательствах, представлены в таблице 3.
Таблица 3. Лечение АГ в сочетании с различными формами ИБС (по AHA/ACC/ASH Scientific Statement, 2015) [19]
|
Нозоло-
гическая форма
|
иАПФ/ АРА
|
Диуретики
|
Недигидропиридино-вые АК
|
БАБ
|
Дигидропиридиновые АК
|
Нитраты
|
Антагонисты альдостерона
|
Гидралазин/ Изосорбит динитрат
|
|
стабильная БКА
|
11
|
12
|
23
|
1
|
2
|
1
|
2
|
не показан
|
|
ОКС
|
11
|
12
|
23
|
14
|
2
|
2
|
25
|
|
ХСН
|
1
|
12
|
не показан
|
16
|
не показан
|
2
|
15
|
2
|
Примечания: иАПФ – ингибиторы ангиотензинпревращающего фермента (иАПФ); АРА – антагонисты рецепторов ангиотензина II; БАБ – бета-адреноблокаторы; АК – антагонисты ионов кальция; 1 – препарат выбора; 2 – дополнительный препарат или альтернативный препарат или специальные показания; 1 – особенно эффективны и показаны у лиц, перенесших ИМ, имеющих систолическую дисфункцию ЛЖ, сахарный диабет (СД), хроническую болезнь почек (ХБП) с протеинурией; 2 – петлевые диуретики могут использоваться при наличии ХСН III–IV функционального класса (ФК) по классификации NYHA или ХБП со снижением скорости клубочковой фильтрации (СКФ)<<0 мл/мин/1,73 м2. Избегать при наличии ХСН с сохранной фракцией выброса (ФВ) ЛЖ; 3 – БАБ противопоказаны; могут быть заменены на недигидропиридиновые АК при условии отсутствия дисфункции ЛЖ или ХСН. Избегать комбинации с БАБ; 4 – внутрь предпочтительно метопролол или бисопролол; 5– спиронолактон или эплеренон при наличии дисфункции ЛЖ, ХСН, СД; 6– карведилол или метопролола сукцинат или бисопролол.
Рекомендации ЕSС (2018) относительно предпочтительности использования тех или иных классов лекарственных средств для лечения АГ изложены в таблице 4.
Таблица 4. Стратегия использования лекарственных средств для лечения АГ (ESC, 2018)
|
Рекомендация
|
Класс
|
Уровень
доказанности
|
|
Среди антигипертензивных лекарственных средств иАПФ, АРА, БАБ, АК и диуретики (тиазидоподобные – хлорталидон и индапамид) в рандомизированных клинических исследованиях продемонстрировали эффективное снижение АД, снижение числа неблагоприятных сердечно-сосудистых событий, вследствие чего они показаны в качестве базисной антигипертензивной стратегии лечения
|
I
|
A
|
|
Комбинированная терапия в качестве начальной терапии рекомендована у большинства пациентов с АГ в качестве начальной терапии. Предпочтительны комбинации средств, влияющих на активность РААС (иАПФ или АРА) и АК или диуретиков. Могут быть использованы комбинации любых других из 5 основных классов антигипертензивных препаратов*
|
I
|
A
|
|
В отдельных клинических ситуациях (стенокардия, перенесенный ИМ, ХСН), а также для контроля ЧСС и для лечения АГ могут быть использованы БАБ в комбинации с любыми другими из 5 основных классов препаратов
|
I
|
A
|
|
Рекомендовано начинать антигипертензивное лечение с двойной комбинации лекарственных средств (предпочтительно с использованием фиксированных комбинаций). Исключение составляют пожилые пациенты и лица с АГ 1 степени и низким риском (особенно при уровне САД <150 мм рт. ст.)
|
I
|
B
|
|
Если АД не контролируется с помощью двойной комбинации, необходимо перейти
на тройную комбинацию (обычно это блокаторы РААС + АК + тиазидный/тиазидоподобный диуретик).
Предпочтительно использовать фиксированные комбинации лекарственных средств
|
I
|
A
|
|
Если АД не контролируется с помощью тройной комбинации, лечение должно быть усилено: добавлен спиронолактон (при непереносимости – другие диуретики в максимальных дозах), БАБ или альфа-адреноблокаторы
|
I
|
B
|
Примечание: * – 5 основных классов антигипертензивных препаратов: иАПФ, АРА, АК, тиазидные и тиазидоподобные диуретики; БАБ
Перспективным для лечения АГ в сочетании со стабильной БКА является использование лекарственных средств, не имеющих выраженного коронароактивного действия, однако, влияющих на ключевой патофизиологический механизм – активность РААС. В нескольких крупных исследованиях (HOPE, SAVE, EUROPA) было доказано, что использование иАПФ способствует уменьшению частоты развития неблагоприятных клинических исходов у лиц с установленным диагнозом стабильной БКА за счет наличия дополнительного, не связанного со снижением АД, кардиопротекторного действия [13–15].
!!!NB: иАПФ должны быть назначены у всех пациентов со стабильной БКА, имеющих сопутствующую АГ, СД, ФВ ЛЖ ≤40% или ХБП при отсутствии противопоказаний (класс I, уровень доказанности А).
Однако важным является следующий вопрос: кардиопротективное действие иАПФ – класс-эффект, присущий всем представителям данной группы лекарственных средств, или кардиопротекция – удел лишь отдельных представителей этого класса антигипертензивных препаратов.
Убедительные доказательства наличия собственно кардиопротективного эффекта и пользы у пациентов с хронической ИБС (включая стабильную БКА)получены в исследовании EUROPA. Скринировано 13 655 пациентов с доказанной хронической ИБС: 64% до включения в исследование перенесли ИМ, ангиографически доказанная БКА имела место у 61%, реваскуляризация выполнена у 55%, только положительный результат стресс-теста имели 5% обследованных. Рандомизировано 12 218 пациентов (средний возраст – 60 лет): 6110 – на прием периндоприла, 6108 – в группу плацебо. Средняя длительность наблюдения составила 4,2 года. Первичная конечная точка: СС смерть, ИМ, остановка сердца. Несмотря на довольно незначительное снижение АД (в среднем – САД -5 мм рт. ст., ДАД -2 мм рт. ст.), в группе оригинального периндоприла (Престариум) имело место существенное достоверное снижение на 20% частоты первичной конечной точки в сравнении с плацебо. Кроме того, отмечалось существенное снижение риска развития повторного ИМ – на 24%, а также числа случаев развития новой СН – на 39%. Среди пациентов со стабильной БКА без ХСН Престариум способствовал существенному улучшению прогноза. Был сделан вывод, что необходимо пролечить Престариумом 50 пациентов в течение 4 лет для предотвращения 1 «большого» неблагоприятного сердечно-сосудистого события, поэтому периндоприл следует включить в схему лечения всех пациентов со стабильной БКА [9].
Однако в исследовании PEACE с трандолаприлом существенного улучшения сердечно-сосудистых исходов в течение 4,8 года наблюдения не выявлено, несмотря на схожее с EUROPA и HOPE снижение САД/ДАД в среднем на 4,4/3,6 мм рт. ст., что обусловливает наличие вопросов о класс-эффекте защитного действия и АПФ [19].
Возможность использования БАБ в качестве антигипертензивных лекарственных средств широко дискутировалась. Однако полученные в многочисленных рандомизированных клинических исследованиях данные свидетельствуют об эффективности данного класса препаратов не только в снижении АД, но и в улучшении прогноза, особенно у отдельных категорий пациентов.
По данным мета-анализа 37 РКИ установлено, что у пациентов с АГ и ИБС частота сердечно-сосудистых осложнений при применении БАБ уменьшалась более выраженно (на 29%), чем при использовании других антигипертензивных препаратов (на 15%, р<0,001) [13].
Целью исследования [18] явилась оценка возможностей БАБ для улучшения прогноза у пациентов с ОКС и сохраненной ФВ ЛЖ. В исследование включено 3236 пациентов с ОКС и ФВ ЛЖ ≥50%. Из них ранее 30% перенесли ИМ с подъемом сегмента ST, у 70% выполнены чрескожные коронарные вмешательства (ЧКВ), из которых в 45% случаев реваскуляризация была полной. Длительность наблюдения составила 9 лет. В группе принимавших БАБ наблюдалось снижение смертности на 29%. При этом прием БАБ был независимым предиктором улучшения отдаленного прогноза после перенесенного ОКС [18].
Улучшение прогноза на фоне терапии БАБ установлено и у пациентов, перенесших коронарное шунтирование (КШ). В когортное 3-летнее исследование во-шли 5926 пациентов с хронической ИБС, перенесшие КШ. У 2514 (42%) из них в анамнезе имел место ИМ. Постоянный прием БАБ способствовал снижению частоты кардиальных и цереброваскулярных осложнений в отдаленные сроки после проведения вмешательства [27].
Согласно Рекомендациям АСС/АНА (2015), БАБ обязательно должны использоваться для лечения АГ у лиц, перенесших ИМ, имеющих дисфункцию ЛЖ как при наличии, так и в отсутствие симптомов ХСН (за исключением наличия противопоказаний). У лиц, имеющих АГ, ИБС и ХСН, карведилол, метопролола сукцинат и бисопролол способствуют улучшению прогноза (табл. 3, 4).
Эксперты Европейского общества кардиологов (2018) рекомендуют использовать БАБ в комбинации с блокаторами РААС (иАПФ/АРА) для лечения АГ у лиц, перенесших ИМ (класс I, уровень доказанности А).
Для антигипертензивного лечения у лиц, имеющих симптомы стенокардии, рекомендовано использовать БАБ и/или АК (класс I, уровень доказанности А).
Аналогичного мнения относительно целесообразности использования средств, влияющих одновременно на активность РААС и СА, придерживаются эксперты и других национальных кардиологических сообществ.
Канадские рекомендации по лечению АГ (CHEP Guidelines, 2016): «У пациентов с АГ, недавно перенесших инфаркт миокарда, начальная терапия должна включать как БАБ, так и иАПФ (класс рекомендаций – A)» [15].
Польские рекомендации по лечению АГ (2015): «У пациентов с АГ и заболеванием сердца (ИБС, сердечная недостаточность) в качестве предпочтительной применяется сочетанная терапия иАПФ и БАБ» [22].
Таким образом, у большинства пациентов с различными формами хронической ИБС (от стабильной БКА до перенесенного ИМ и реваскуляризации миокарда) в многочисленных РКИ доказана эффективность как иАПФ, так и БАБ, как для уменьшения симптомов, так и для улучшения прогноза. Оба класса лекарственных средств входят в многочисленные клинические рекомендации (и международные, и национальные). Однако относительно кардиопротективного действия сочетание иАПФ и БАБ известно меньше.
Престилол – первый и единственный комбинированный препарат, содержащий в одной таблетке два лекарственных средства, обладающих доказанным кардио-протективным действием – высокоселективный ?1-адреноблокатор бисопролол и современный иАПФ – периндоприл.
Периндоприл (Престариум) способствует снижению уровня АТ II, увеличению содержания брадикинина. Преимуществом периндоприла перед другими иАПФ является тканевая (в первую очередь, кардио-) селективность, которая обеспечивается благодаря высокой липофильности [7], высокое отношение селективности брадикинина/ангиотензина I [6, 14], сосудистые противовоспалительные свойства [7]. Периндоприл обладает отношением остаточного действия к максимальному, близким к 100, что обеспечивает, наличие эффекта, как минимум, в течение 24 часов.
Бисопролол обусловливает уменьшение ответной реакции симпатического отдела вегетативной нервной системы, снижение ЧСС и УО и, как следствие, уменьшение АД и потребности миокарда в кислороде, удлинение фазы диастолы и улучшение коронарной перфузии, а также снижение активности ренина в плазме. Преимуществом бисопролола перед другими БАБ является наличие кардиоселективности без внутренней симпатомиметической активности, отсутствие отрицательного влияния на метаболизм углеводов и липидный обмен, длительный период полувыведения, обусловливающий 24-часовую эффективность.
Весьма впечатляющими оказались результаты субанализа исследования EUROPA [4]. Было установлено, что при включении в исследование БАБ принимали 7534 пациента, что составило 62%. Сочетанное применение БАБ и Престариума в сравнении с монотерапией БАБ способствовало уменьшению числа случаев развития фатального и нефатального ИМ на 28% (р=0,001), частоты госпитализации по поводу ухудшения течения СН на 45% (р=0,025), а также снижение на 24% комбинированной конечной точки, включавшей смерть от осложнений ССЗ, нефатальный ИМ и остановку сердца с успешной реанимацией (р=0,002).
Таким образом, было установлено кумулятивное положительное влияние сочетанного применения лекарственных средств с кардиопротективным действием – БАБ и оригинального периндоприла на прогноз у пациентов с различными формами хронической ИБС.
Еще более убедительные данные были получены [5] при проведении ретроспективного объединенного анализа трех крупнейших клинических исследований, посвященных эффективности периндоприла у пациентов очень высокого риска: ADVANCE (11 440 пациентов с сахарным диабетом 2-го типа, EUROPA – 2218 человек с различными формами хронической ИБС и PROGRESS – 6105 пациентов, перенесших инсульт или ТИА (всего 29 463 пациента, средняя продолжительность наблюдения – 4 года). При включении в исследование уже 11 418 (38,8%) пациентов принимали БАБ. Было установлено, что добавление Престариума к БАБ у пациентов высокого риска способствовало снижению риска развития неблагоприятных сердечно-сосудистых событий – композитной первичной точки (сердечно-сосудистая смертность, нефатальный ИМ и инсульт) на 20% и вторичной конечной точки – нефатальный ИМ, сердечно-сосудистая и общая смертность на 23%. Наиболее выраженный эффект наблюдался у пациентов с АГ – частота первичной конечной точки снижалась на 23%, риск нефатального ИМ – на 26%, смертность от любых причин – на 32%. Авторы сделали вывод, что добавление периндоприла к терапии БАБ имеет хорошо документированный дополнительный защитный эффект к доказанной кардиопротекции, обеспеченной приемом только БАБ [5].
Еще одной нерешенной проблемой ведения пациентов с АГ в сочетании с различными формами хронической ИБС является низкая приверженность к лечению, которая способствует развитию таких неблагоприятных клинических исходов, как повторная госпитализация, ИМ и смерть. Причем это является проблемой не только пациентов и врачей, но и систем здравоохранения в целом, так как при этом существенно повышается стоимость лечения указанной категории пациентов [3, 17].
Каждый четвертый пациент с ИБС не соблюдает предписанный режим терапии ?-адреноблокатором и/или иАПФ. По данным ретроспективного когортного исследования, включавшего 15 767 пациентов с ИБС, которых наблюдали в среднем 4 года, низкая приверженность терапии БАБ и иАПФ имела место лишь у 29% и 22% лиц соответственно [11].
Назначение фиксированных комбинаций лекарственных средств существенно повышает приверженность к терапии и, как следствие, эффективность лечения. Результаты мета-анализа S.Bangalore [2] подтвердили, что применение комбинированных препаратов, содержащих в одной таблетке два лекарственных средства, при АГ снижает риск несоблюдения предписанного режима терапии на 24% по сравнению с применением свободных комбинаций препаратов, что в совокупности делает Престилол еще более привлекательным в комплексной терапии АГ в сочетании с различными формами хронической ИБС (в том числе стабильной БКА).
Выводы:
1. Престилол – первая и единственная фиксированная комбинация современного иАПФ периндоприла, обладающего высокими кардиопротективными свойствами, и высококардиоселективного БАБ – бисопролола, также имеющего хорошо доказанное защитное действие в отношении предупреждения развития неблагоприятных сердечно-сосудистых событий у пациентов с болезнями системы кровообращения на всех этапах сердечно-сосудистого континуума.
2. ПРЕСТИЛОЛ оказывает влияние на симпатоадреналовую и ренин-ангиотензин-альдестероновую системы, играющие ключевую роль в патогенезе развития как АГ, так и стабильной стенокардии – симпатоадреналовую и ренин-ангиотензин-альдостероновую.
3. Мета-анализ трех крупнейших исследований EUROPA, ADVANCE и PROGRESS показал, что комбинация иАПФ периндоприла и БАБ обеспечивает дополнительную защиту у пациентов высокого риска, особенно выраженную у лиц с АГ – присоединение оригинального периндоприла к приему БАБ позволило снизить риск развития нефатального ИМ на 26%, смертности – на 32%.
4. Для пациентов, имеющих сочетание АГ и стабильной стенокардии, использование фиксированной комбинации БАБ и иАПФ, Престилол, благодаря двойной кардиопротекции открывает новые возможности как для контроля АД, так и для защиты от развития неблагоприятных сердечно-сосудистых событий, таких как ИМ, смерть от сердечно-сосудистых заболеваний, развитие и прогрессирование ХСН.
5. Согласно Рекомендациям ESC и ACC/AHA, БАБ и иАПФ являются обязательными компонентами терапии пациентов с АГ в сочетании с различными формами стабильной хронической ИБС.
6. Использование фиксированной комбинации периндоприла с бисопрололом в 1 таблетке Престилол в комплексной терапии АГ в сочетании с различными формами хронической ИБС способствует повышению приверженности пациентов к лечению и, как следствие, увеличению медицинской и социально-экономической эффективности лечения указанной категории пациентов.
Л И Т Е Р А Т У Р А
1. Подзолков В.И. // РМЖ. – 2008. – Т.11, №16. – С.1517–1523.
2. Bangalore S., et al. // Am. J. Med. – 2007. – Vol.120, N8. – P.713–719.
3. Baroletti S., Dell’Orfano H. // Circulation. – 2010. – Vol.121. – P.1455–1458.
4. Bertrand M.E., et al. // Am. Heart. J. – 2015. – Vol.170. – P.1092–1098.
5. Brugts J.J., et al. // Eur. Heart J. – 2009. – Vol.30. – P.1385–1394.
6. Chobanian A.V., Bakris G.I., Black H.R., et al. // Hypertension. – 2003. – Vol.42. – P.1206–1252.
7. DiNicolantonio J.J., et al. // Postgrad. Med. – 2013. – Vol.125, N4. – P.154–168.
8. Dzau V. // Am. Heart J. – 1991. – P.1244–1263.
9. Fox K.M. // Lancet. – 2003. – Vol.362. – P.782–788.
10. Global Burden of Disease Study 2013 Collaborators. // Lancet. – 2015. – Vol.386, N9995. – P.743–800.
11. Ho P.M., et al. // Am. Heart J. – 2008. – Vol.155. – P.772–779.
12. Izzo J.L., Gradman A.H. // Med. Clin. North Am. – 2004. – Vol.88. – P.1257–1271.
13. Komajda M., et al. // Eur. Heart J. – 2016. – Vol.37, N2. – P.152–160.
14. Law M.R., et al. // BMJ. – 2009. – Vol.338. – b1665.
15. Leung A.A., et al. // Can. J. Cardiol. – 2016. doi:10.1016/j.cjca.2016.02.066
16. Pfeffer M.A., Braunwald E., Moye L.A., et al. // Engl. J. Med. – 1992. – Vol.327. – P.669–677.
17. Piepoli M.F., et al. // Eur. Heart J. – 2016. doi:10.1093/eurheartj/ehw106
18. Raposeiras-Roubin S., et al. // Rev. Esp. Cardiol. – 2015. – Vol.68, N7. – P.585–591.
19. Rosendorff C., et al. // Hypertension. – 2015. – Vol.65, N6. – P.1372–1407.
20. Sipahi I., Tuzcu E.M., Schoenhagen P., Wolski K.E., et al. // J. Am. Coll. Cardiol. – 2006. – Vol.48. – P.833–838.
21. Steg G., et al. // PLoS One. – 2012. – Vol.7, N5. – e36284.
22. Tykarski A., et al. // Kardiol. Pol. – 2015. – Vol.73, N8. – P.676–700.
23. World Health Organization. A global brief on hypertension, 2013. WHO/DCO/WHD/2013.2
24. World Health Organization. The Atlas of Heart Disease and Stroke, 2004.
25. Yusuf S. // Circulation2006. – Vol.113. – P.2166–2168.
26. Yusuf S., Sleight P., Pogue J., et al. // N. Engl. J. Med. – 2000. – Vol.342. – P.145–153.
27. Zhang H., et al. // Circulation. – 2015. – Vol.131. – P.2194–2201.
Медицинские новости. – 2018. – №10. – С. 4-10.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.