Внимание! Статья адресована врачам-специалистам
Rudenka E.V.
Belarusian State Medical University, Minsk
Modern trends in diagnostics, prevention and treatment of vitamin D deficiency
Резюме. Приведен обзор данных литературы о распространенности и причинах гиповитаминоза D в мире и в Республике Беларусь. Выделены факторы риска, влияющие на уровень витамина D в организме человека. Изложены этапы метаболизма витамина D и его основные биологические эффекты. Представлены современные методы лабораторной диагностики уровня витамина D в сыворотке крови. Дана современная концепция клинической интерпретации референсных данных уровней 25(ОН)D. Предложены схемы индивидуальной коррекции дефицита и гиповитаминоза D в группах риска согласно современным международным рекомендациям.
Ключевые слова: витамин D, гиповитаминоз, дефицит витамина D, 25(ОН)D, колекальциферол.
Медицинские новости. – 2020. – №8. – С.31–36.
Sammary. A review of the literature on the prevalence and causes of hypovitaminosis D in the world and the Republic of Belarus is given. Risk factors that affect the level of vitamin D in the human body are identified. The stages of vitamin D metabolism and its main biological effects are described. Modern methods of laboratory diagnosis of the status of vitamin D in blood serum are presented. The concept of the clinical interpretation of reference data of levels 25(OH)D is given. Schemes of individual correction of deficiency and hypovitaminosis D in risk groups according to modern international recommendations are proposed.
Keywords: vitamin D, hypovitaminosis, deficit D, 25(OH)D, colecalciferol.
Meditsinskie novosti. – 2020. – N8. – P.31–36.
В начале XXI века проблема гиповитаминоза D вновь приобрела не только медицинское, но и медико-социальное значение. Согласно статистическим данным, более чем 1 миллиард человек в мире имеют дефицит витамина D (ДВД) или его недостаточность. Исследования, проведенные в Европе по изучению статуса витамина D посредством измерения концентрации общего 25(ОН)D в крови, показали, что только 13% в обследованной популяции имели его субоптимальный уровень [13, 17, 18].
С одной стороны, причинами такой высокой распространенности гиповитаминоза D являются объективные демографические изменения: заметное постарение населения и закономерный рост гериатрической патологии, обусловленной как возрастными нарушениями регуляции функций организма, так и условиями жизни пожилых людей (несбалансированное питание, низкий уровень физической активности, недостаточное пребывание на солнце); с другой – изменения климата, которые во многом связаны с деятельностью человека (увеличение числа облачных дней и уменьшение инсоляции снижают образование витамина D в организме). Изменение зенитного угла солнца в зависимости от географической широты, времени года или времени суток существенно влияет на синтез витамина D3 (колекальциферола). В местностях, находящихся на широтах выше и ниже 33°, выработка колекальциферола в коже происходит с очень низкой интенсивностью или отсутствует в течение большей части зимы [19].
В Республике Беларусь более 50% женщин всех возрастных групп имеют низкий уровень витамина D в сыворотке крови независимо от времени года, у женщин старше 60 лет в осенне-зимний период частота гиповитаминоза D составляет 79%, в весенне-летний – 75%. У пожилых мужчин в осенне-зимний период частота гиповитаминоза D составляет 73%, в весенне-летний – 57% [4, 18].
В последние годы активно изучается генетическая предрасположенность к ДВД. Ген рецептора витамина D (РВД) является одним из центральных регуляторов в эндокринной системе и выступает как ген-кандидат, обусловливающий особенности роста человека. Доказано, что мутации этого гена приводят к развитию рахита, остеомаляции, задержке роста, деформациям костей и вторичному гиперпаратиреозу [13, 19]. Кроме того, новые данные свидетельствуют о вероятной роли полиморфизма РВД в патогенезе повреждений костной ткани и развитии вторичного остеопороза при ревматоидном артрите и других аутоиммунных заболеваниях [14, 15].
Особый интерес в последние десятилетия вызывает изучение роли витамина D и его активных метаболитов в обеспечении функционирования компонентов иммунной системы: лимфоцитов, моноцитов и дендритных клеток. Появились исследования, свидетельствующие о способности 1,25-дигидроксивитамина D3 индуцировать процессы слияния и дифференциации макрофагов, снижать продукцию медиаторов воспаления при аутоиммунных заболеваниях, регулировать клеточный ответ на окислительный стресс [9, 15]. Всего было обнаружено более 30 положительных эффектов витамина D на иммунную систему, что позволяет инициировать дальнейшие исследования по изучению возможностей его применения в терапии аутоиммунных заболеваний [7, 10, 20].
Термин «витамин D» объединяет группу сходных по химическому строению секо-стероидов, среди которых наибольшее применение имеют витамины D2 (эргокальциферол) и D3 (колекальциферол). Эргокальциферол в основном образуется в растениях из эргостерола, а колекальциферол – из 7-дегидрохолестерина в организме человека и животных под воздействием солнечных лучей.
На рисунке 1 представлены этапы образования, метаболизма витамина D и его основные биологические эффекты [5].
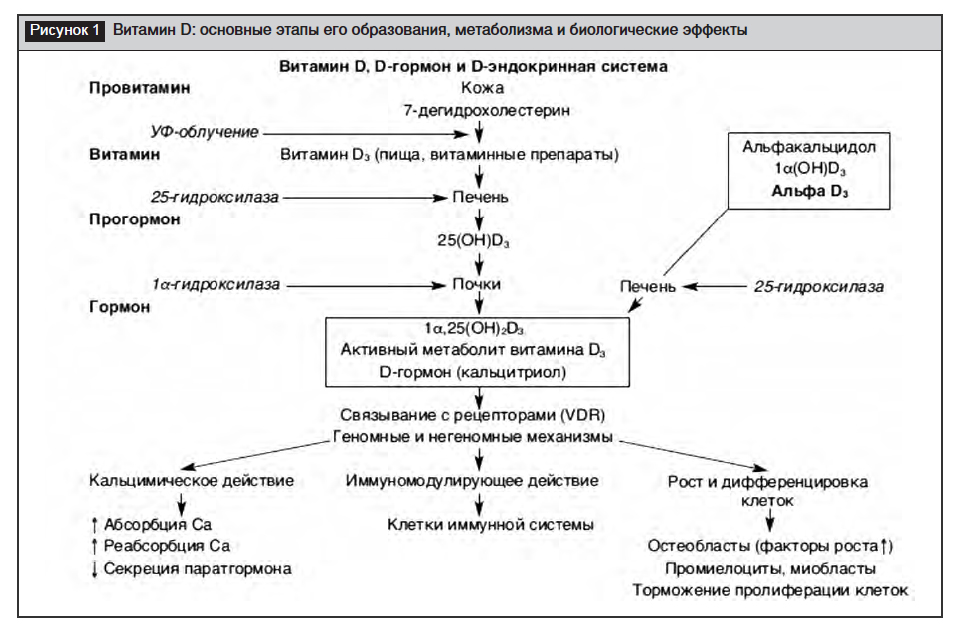
Синтезируемый в коже под воздействием ультрафиолетовых лучей колекальциферол связывается со специфическим витамин D-связывающим белком (транскальциферином) и переносится в печень. Далее в эндоплазматическом ретикулуме гепатоцитов происходит его гидроксилирование по 25-му атому углерода с образованием 25(ОН)D3 (кальцидола), который связывается с ?-глобулином и циркулирует в крови, не влияя на обмен кальция. Следующий этап гидроксилирования уже 25(ОН)D3 под влиянием фермента 1?-гидроксилазы происходит в митохондриях клеток проксимальных канальцев почек. В итоге синтезируется активный метаболит витамина D – 1,25(ОН)2DЗ (кальцитриол) и 24,25(ОН)2D3. Первый из них в последнее время называют D-гормоном, поскольку именно эта форма витамина D участвует в регуляции кальций-фосфорного обмена, а также посредством взаимодействия со специфическими ядерными РВД, расположенными во множестве тканей организма человека, осуществляет различные биологические эффекты, а второй по типу обратной связи управляет концентрацией паратиреоидного гормона (ПТГ) [5, 15].
Так называемые «скелетные эффекты» кальцитриола играют значительную роль в регуляции метаболических процессов, происходящих в костной ткани. Под влиянием D-гормона ускоряются процессы абсорбции кальция в кишечнике и его реабсорбция в почках. Кальцитриол усиливает кишечную абсорбцию кальция в тонком кишечнике за счет стимуляции синтеза в энтероцитах кальций-связывающего белка – кальмодулина. В свою очередь, кальмодулин транспортирует ионы кальция через кишечную стенку и систему лимфатических сосудов и в кровеносное сосудистое русло. Достаточный плазменный уровень кальцитриола повышает эффективность кишечной абсорбции ионизированного кальция в 2–3 раза и фосфора – до 80%. Подобным образом осуществляются процессы реабсорбции кальция и в почечных канальцах.
В костной ткани кальцитриол повышает экспрессию лиганда рецептора-активатора ядерного фактора кВ (RANKL), ускоряет процессы пролиферации остеобластов, синтез остеокальцина, коллагена и гликозаминогликанов. 1,25(OH)2D – мощный стимулятор остеокластогенеза in vitro, при введении высоких доз 1,25(ОН)2D связывается с РВД на остеобластах и увеличивает экспрессию и высвобождение RANKL [9, 10].
Посредством взаимодействия с РВД 1,25(OH)2D3 проявляет свои геномные эффекты в различных органах и клетках, представленных в таблице 1 [5].
Таблица 1. Основные органы и клетки, имеющие РВД
|
Система
|
Орган/ткань/клетка
|
|
Желудочно-кишечный тракт
|
Пищевод, желудок, толстый и тонкий кишечник
|
|
Гепатобилиарная
|
Клетки
|
|
Мочевыделительная
|
Почки, мочеточники, простата
|
|
Сердечно-сосудистая
|
Сердечная мышца
|
|
Эндокринная
|
Гипофиз, щитовидная и паращитовидная железы, надпочечники
|
|
Экзокринные железы
|
Околоушные, сальные
|
|
Репродуктивная
|
Яички, яичники, плацента, матка, эндометрий
|
|
Иммунная
|
Тимус, костный мозг, В- и Т- лимфоциты
|
|
Дыхательная
|
Альвеолярные клетки
|
|
Мышечно-скелетная
|
Остеобласты, остеокласты, остеоциты, поперечно-полосатая мускулатура, хондроциты
|
|
Эпидермис и его производные
|
Кожа, молочные железы, волосяные фолликулы
|
|
ЦНС
|
Мозговые нейроны
|
|
Соединительная ткань
|
Фибробласты, клетки стромы
|
Диагностика дефицита витамина D
В настоящее время клинические отделения лабораторной диагностики оснащаются доступными стандартизованными методами определения его статуса в организме. При лабораторном исследовании необходима проверка надежности используемого в клинической практике метода определения 25(OH)D (по международной аббревиатуре) относительно международных стандартов (DEQAS, NIST), с использованием того же метода в условиях одной и той же лаборатории. Выявление ДВД осуществляется с применением наборов реагентов для определения концентрации общего 25(OH)D, включающего 25(OH)D2 и 25(OH)D3 в сыворотке крови. В клинической практике в настоящее время применяются современные методы масс-спектрометрии, конкурентного связывания с белком, высокоэффективной жидкостной хроматографии, радиоиммунного, иммуноферментного или иммуннохемилюминесцентного анализа. Для оценки статуса витамина D при применении препаратов колекальциферола рекомендуется проводить забор крови не менее чем через 3 дня после последнего приема препарата. Определение концентрации общего 25-гидроксивитамина D, циркулирующего в крови, сегодня является лучшим методом для оценки и мониторинга статуса витамина D в клинической практике, поскольку имеет длительное время полувыведения – около 15–16 дней [13]. Сывороточная концентрация общего 25-гидроксивитамина D в зависимости от метода измерения выражается в нанограммах на миллилитр (нг/мл) или в наномолях на литр (нмоль/л). Для сравнения результатов следует учитывать, что 1 нг/мл равняется 2,5 нмоль/л. Показатели уровней 25(OH)D вариабельны и в значительной степени зависят от методов диагностики, географического расположения страны, технических ошибок, человеческого фактора. Для уточнения патологии костной ткани, обусловленной дефицитом витамина D, необходимо оценить уровни ПТГ, кальция, фосфора, ОЩФ, магния, маркера резорбции костной ткани – С-концевого телопептида коллагена I типа (?-Cross Laps), маркеров формирования костного матрикса P1NP (N-терминальный пропептид проколлагена 1-го типа, Total P1NP) или остеокальцина в сыворотке крови, соотношение кальций/креатинин в утренней моче. При уровне 25(ОН)D менее 10 нг/мл необходимо углубленное обследование больного для исключения остеомаляции (биопсия крыла подвздошной кости), наследственных заболеваний соединительной ткани (генетическое тестирование), определение уровней 1,25(ОН)2D при наличии хронических заболеваний почек. Для исключения нарушений процессов всасывания в кишечнике важно определить маркеры целиакии и других хронических воспалительных заболеваний желудочно-кишечного тракта [5, 9, 19].
Референсные данные уровней 25(ОН)D и их интерпретация представлены в таблице 2. Данная концепция клинической интерпретации концентраций кальцидола была разработана большой группой ученых с 2011 по 2013 год под руководством профессора П. Плудовского и опубликована в Практических рекомендациях по поступлению витамина D и лечению его дефицита в странах Центральной Европы [16].
Таблица 2. Клиническая интерпретация референсных показателей 25 (ОН)D в сыворотке крови
|
Концентрация 25(ОН)D
в сыворотке
|
Клиническая интерпретация
|
|
Менее 20 нг/мл
(50 нмоль/л)
|
Отражает дефицит витамина D; требует медикаментозного лечения
|
|
20–30 нг/мл
(50–70 нмоль/л)
|
Отражает субоптимальный статус обеспеченности витамином D; требует умеренного повышения дневной дозы витамина D
|
|
30–50 нг/мл
(75–125 нмоль/л)
|
Отражает адекватный статус обеспеченности витамином D; требует сохранения применяемой схемы обеспечения витамином D и принимаемой дозы
|
|
50–100 нг/мл
(125–250 нмоль/л)
|
Отражает высокий уровень поступления витамина D; требует поддержания принимаемой дозы обеспечения витамином D
при низких значениях этого интервала или умеренного снижения дозы – при высоких значениях интервала
|
|
Выше 100 нг/мл
(250 нмоль/л)
|
Угрожающий для общих показателей здоровья уровень; требует снижения/прекращения поступления витамина D в организм до момента достижения целевых концентраций
|
|
Выше 200 нг/мл
(500 нмоль/л)
|
Считается токсичной концентрацией, требует прекращения поступления витамина D в организм до момента достижения целевых концентраций обеспеченности витамином D; могут потребоваться специфические лечебные мероприятия для коррекции токсических эффектов
|
Показания для определения 25(ОН)D в сыворотке крови
1. Пожилые люди, длительно проживающие в закрытом помещении.
2. Для дифференциальной диагностики метаболических заболеваний скелета (рахит, остеомаляция, остеодистрофии, остеопороз и др).
3. Выявление аутоиммунных и онкологических заболеваний.
4. Выраженные дефицит или избыточная масса тела/ожирение.
5. Целиакия, мальабсорбция.
6. Перед назначением препаратов для лечения остеопороза.
7. Менопауза у женщин, гипогонадизм у мужчин.
8. Оценка динамики при применении высоких доз витамина D.
9. Беременность и лактация.
10. Избыточная масса тела.
11. Наличие других факторов риска ДВД.
В 2013 году Министерством здравоохранения Республики Беларусь была утверждена Инструкция по применению «Методы диагностики, профилактики и дифференцированного лечения дефицита витамина D» №033-031313 от 14.06.2013 г. [3]. Приложением к этой инструкции является алгоритм диагностики и профилактики ДВД, которым можно руководствоваться для выявления групп риска, определения показаний к исследованию плазменного уровня 25(ОН)D, а также для установления необходимой дозы колекальциферола (рис. 2).

Способы коррекции дефицита витамина D
1. Поступление с продуктами питания.
2. Фортификация продуктов питания колекальциферолом.
3. Достаточное естественное солнечное облучение (основной источник).
4. Применение ультрафиолетовых ламп.
5. Прием эргокальциферола внутрь (D2).
6. Прием лекарственных форм колекальциферола внутрь (D3).
7. Применение активных метаболитов витамина D.
8. Парентеральное введение препаратов витамина D.
Рекомендации по диетическому питанию
Употребляя продукты растительного и животного происхождения, за сутки человек получает не более 100–200 МЕ. Макрель, лосось, тунец, скумбрия и сельдь являются источниками витамина D. Также богаты витамином D печень трески и палтуса, икра, морепродукты, шпроты в масле, говяжья и свиная печень, сырые яичные желтки, сыр, сливочное масло. Наибольшее содержание витамина D в рыбьем жире, в 100 граммах которого – 250 мкг витамина. Из продуктов растительного происхождения, содержащих витамин D, следует отметить картофель, петрушку, орехи, семечки, грибы, овсянку, а также такие растения, как крапива, хвощ, зелень одуванчика и люцерна.
Во многих странах осуществляется фортификация некоторых наиболее употребляемых населением продуктов: муки, хлеба, молока, соков, йогурта, растительных масел и др. В Великобритании были проведены исследования, по экономической оценке, обогащения пшеничной муки добавками витамина D. В результате был доказан веский экономический аргумент в пользу обогащения пшеничной муки витамином D (9,5 фунтов стерлингов за QALY). Ученые подсчитали, что только обогащение пшеничной муки привело к снижению гиповитаминоза у населения страны на 25% [6].
Роль солнечного излучения
Главным источником витамина D для человека является его образование при воздействии на кожу солнечных лучей, особенно, весной и летом, когда наблюдается наибольшее число часов солнечного сияния. Витамин D, образовавшийся в коже, может оставаться в крови минимум в два раза дольше, чем поступающий с пищей. При получении взрослым человеком, одетым в купальный костюм, одной минимальной эритемной дозы ультрафиолетового излучения (небольшое порозовение кожи через 24 ч после воздействия) количество производимого витамина D эквивалентно приему внутрь 10 000–25 000 МЕ. На процессы синтеза колекальциферола в кожных покровах человека может влиять множество факторов, наиболее значимые из них: использование солнцезащитных средств, кожная пигментация, наличие шрамов после ожогов, псориаза, снижение содержания 7-дегидрохолестерола в коже у пожилых, время года, географическое положение, продолжительность светового дня и др. [6, 8, 19].
Фармакологическая коррекция гиповитаминоза D
Колекальциферол и его активные метаболиты поступают в аптечную сеть в виде растворов, капсул, таблеток в дозировках от 200 МЕ до 50 000 МЕ. В клинической практике врачей различных специальностей в качестве монотерапии ДВД в зависимости от исходной концентрации 25(ОН)D могут применятся как высокие дозы по индивидуальным схемам коррекции, так и более низкие профилактические и лечебные (от 500 до 2000 МЕ), которые не требуют лабораторного мониторинга статуса витамина D, в том числе и в комбинации с препаратами кальция.
В таблице 3, составленной на основании обобщения данных, полученных при изучении международных рекомендаций по диагностике и коррекции гиповитаминоза D, приводятся показания для назначения витамина D3 в различных дозах в зависимости от исходных показателей 25(ОН)D и частота лабораторного контроля для мониторинга его статуса с целью уточнения необходимости коррекции проводимой терапии и исключения возможной передозировки колекальциферола [1, 9, 12].
Таблица 3. Показания для назначения профилактических и лечебных доз витамина D3
|
Доза колекальциферола
|
Показания к применению
|
Примечания
|
|
200–400–500 МЕ
в поливитаминных
комплексах
|
Профилактика гиповитаминоза, укрепление иммунитета
в дозах до 800–1000 МЕ в сутки
|
Для здоровых людей без контроля 25(ОН)D
|
|
400 МЕ в комплексе
с солями кальция
|
Профилактика остеопороза. Лечение остеопороза
в комплексе с антирезорбтивными препаратами
с дополнением витамина D до 2000 МЕ в сутки
|
Контроль 25(ОН)D перед назначением антирезорбентов
|
|
500 МЕ
водорастворимый
раствор 1 капля
|
Профилактика и лечение остеопороза в суточных дозах до 4000 МЕ вместе с комбинированными препаратами кальция и витамина D. Лечение остеомаляции
|
Контроль 25(ОН)D 1 раз в 6 месяцев при выявлении ДВД
и назначении более 2000 МЕ в сутки
|
|
500 МЕ
жирорастворимый
раствор 1 капля
|
Профилактика и лечение остеопороза в суточных дозах от 1000 до 4000 МЕ вместе c комбинированными
препаратами кальция (500 мг) и витамина D (400 МЕ)
|
Контроль 25(ОН)D 1 раз в 6 месяцев при выявлении ДВД
и назначении более 2000 МЕ в сутки
|
|
500 МЕ жевательные
капсулы
|
Профилактика и лечение остеопороза в суточных дозах до 4000 МЕ + препараты кальция и витамина D (400 МЕ). Лечение остеомаляции
|
Контроль 25(ОН)D 1 раз в 6 месяцев при назначении
доз более 2000 МЕ и дальнейшим его мониторингом по показаниям
|
|
2000 МЕ
желатиновые капсулы
|
Профилактика и лечение ДВД в суточных дозах до 4000 МЕ. Лечение остеомаляции
|
При исходных уровнях 25(ОН)D меньше 20 нг/мл с контролем 25(ОН)D 1 раз в 6 месяцев
|
|
5000 МЕ
желатиновые капсулы
|
Лечение ДВД в суточных дозах до 5000–10 000 МЕ. Лечение остеомаляции
|
Контроль 25(ОН)D 1 раз в 3 месяца
|
|
10 000 МЕ
желатиновые капсулы
|
Лечение ДВД в суточных дозах по 10 000 МЕ при уровне 25(ОН)D меньше 10 нг/мл
|
Контроль 25(ОН)D через 2 недели от начала приема
с последующей коррекцией дозы, контроль кальция в сыворотке крови. Превышение данной дозы в сутки не рекомендуется
|
|
50 000 МЕ
желатиновые капсулы, таблетки
|
Лечение ДВД индивидуально 1 раз в неделю
на 7–8 недель при уровнях 25(ОН)D 10 нг/мл и меньше
|
Контроль 25(ОН)D 1 раз в 3 месяца для подбора оптимальной поддерживающей дозы, контроль кальция в сыворотке крови
|
|
50 000 МЕ
желатиновые капсулы, таблетки
|
1 раз в месяц при уровне 25(ОН)D меньше 30 нг/мл
для профилактики гиповитаминоза D
|
Контроль 25(ОН)D при наличии факторов риска
гиповитаминоза D, контроль кальция в сыворотке крови
|
Примечание: при достижении целевого уровня 25(OH)D 30–40 нг/мл на фоне приема высоких доз витамина D можно перейти на прием поддерживающих доз 1500–2000 МЕ в сутки.
Согласно практическим рекомендациям, предложенным Институтом медицины США в 2011 году, для профилактики ДВД может быть рекомендован дифференцированный подход к назначению суточных доз колекальциферола от 400 МЕ до 10 000 МЕ [12]. Некоторые аспекты из этих рекомендаций представлены ниже.
Для здоровой популяции в возрасте 18–50 лет с целью профилактики ДВД рекомендуется получать не менее 600–800 МЕ витамина D в сутки для достижения субоптимальных уровней 25(OH)D более 20 нг/мл. Чтобы поддерживать концентрацию 25(ОН)D более 30 нг/мл, нужно принимать 1500–2000 МЕ колекальциферола в сутки.
Лицам старше 50 лет для профилактики ДВД необходимо не менее 800–1000 МЕ витамина D в сутки.
В последних мета-анализах на основе двойных слепых РКИ было показано, что в популяции пожилых мужчин и женщин дополнительный прием витамина D в дозе 800–1000 МЕ приводил к снижению любых невертебральных переломов, переломов бедра и падений приблизительно на 20%.
Научные исследования у лиц старше 65 лет по изучению влияния 800 МЕ витамина D в сутки на мышечную силу, нарушения координации движений и частоту падений выявили следующие результаты: мышечная сила повысилась на 4–7%; координация движений улучшилась на 28% а частота падений снижалась до 35–72% по данным различных источников.
Беременным и кормящим женщинам для профилактики ДВД необходимо не менее 800–1200 МЕ витамина D в сутки. При наличии факторов риска ДВД следует оценить исходный уровень 25(OH)D, в зависимости от его показателей, подобрать дозу от 1500–4000 МЕ в сутки с последующим контролем за динамикой 25(ОН)D 1 раз в 3–6 месяцев.
Лицам с избыточной массой тела или с мальабсорбцией суточные дозы витамина D3 могут быть увеличены до 4000 и более в сутки.
В таблице 4 дана характеристика зарегистрированных Министерством здравоохранения Республики Беларусь отечественной фармацевтической компании УП «Минскинтеркапс» форм выпуска препаратов колекальциферола с различными дозами, что позволяет назначать индивидуальную схему лечения ДВД в зависимости от конкретной клинической ситуации [20].
Тпблица 4. Препараты колекальциферола фармацевтической компании «Минскинтеркапс»
|
Название препарата
|
Фармакотерапевтическая группа
|
Форма выпуска
|
Доза
|
|
Д3-КАПС УЛЬТРА
|
Витамин D и его аналоги.
Колекальциферол.
Код АТХ A11CC05
|
Капсулы жевательные, масляный раствор колекальциферола
1 млн МЕ / 1 г
|
12,5 мкг (500 МЕ)
|
|
Д3-КАПС
|
Витамин D и его аналоги.
Колекальциферол.
Код АТХ A11CC05
|
Масляный раствор колекальциферола
1 млн МЕ / 1 г
|
50 мкг (2000 МЕ)
125 мкг (5000 МЕ)
|
|
Д3-КАПС МАКСИМА
|
Витамин D и его аналоги.
Колекальциферол.
Код АТХ A11CC05
|
Масляный раствор колекальциферола
1 млн МЕ / 1 г
|
1,25 мг (50 000 МЕ)
|
Примечание: 1 мкг =40 МЕ.
В результате приема высоких доз колекальциферола на протяжении длительного периода повышается риск его передозировки, клиническими признаками которой являются анорексия, тошнота, полиурия, запоры, слабость, потеря веса, головная боль, депрессия, жажда, ригидность мышц, кальцификация мягких тканей, нефрокальциноз, повышение артериального давления.
Лабораторными признаками, подтверждающими передозировку витамина D, являются гиперкальциемия, гиперкальциурия (отношение Са/креатинин мочи более 0,57), повышение уровня 25(OH)D выше 100 нг/мл. Гиперкальциемический криз, развивающийся при повышении уровня кальция в крови до 4 ммоль/л, может привести к летальному исходу в результате угнетения нервной деятельности и комы.
Препараты витамина D3 противопоказаны пациентам с гиперкальциемией, гиперкальциурией, нефролитиазом, склонностью к аллергическим реакциям на компоненты состава лекарственного средства. В связи с повышенным риском гиперкальциемии и гиперкальциурии препараты витамина D не назначаются при диагностированных гранулематозах, саркоидозе, метастазах в кости, синдроме Вильямса [2, 5, 9].
Заключение
При назначении препаратов витамина D лечащий врач должен приложить максимум усилий для достижения адекватной приверженности к лечению и получения наилучшего результата в отношении первичной и вторичной профилактики гиповитаминоза витамина D и связанных с ним осложнений. В то же время необходим регулярный лабораторный мониторинг показателей кальций-фосфорного обмена для исключения гиперкальциемии, особенно при назначении высоких доз витамина D. Монотерапия ДВД колекальциферолом проводится годами, а при отсутствии эффекта и в некоторых конкретных клинических ситуациях, особенно при почечных остеодистрофиях, назначаются его активные метаболиты кальцитриол или альфакальцидол. Более подробную информацию о биологических эффектах витамина D можно получить на сайте https://vitamindwiki.com.
Л И Т Е Р А Т У Р А
1. Дефицит витамина D у взрослых: диагностика, лечение и профилактика. Российская ассоциация эндокринологов. – 2015. http://specialist.endocrincentr.ru. – Дата доступа: 15.05.2016.
2. Инструкция по применению Инструкция по применению препаратов Д3-капс. – https://www.rceth.by/NDfiles/instr/19_09_2965_s.pdf, https://www.rceth.by/NDfiles/instr/19_09_2963_s.pdf, https://www.rceth.by/NDfiles/instr/19_09_2964_s.pdf.
3. Методы диагностики, профилактики и дифференцированного лечения дефицита витамина D. Инструкция по применению регистрационный №033-0313: утв. 14.06.2013 / Э.В. Руденко, Н.С. Сердюченко, Л.И. Алехнович, Г.Н. Романов, Е.В. Руденко, О.Ю. Самоховец, Е.А. Василенко. – Минск, 20013. – 15 с.
4. Руденко Э.В. и др. // Лабораторная диагностика: Восточная Европа. – 2013. – №2. – С.53–60.
5. Шварц Г.Я. // Український ревматологічний журнал. – 2009. – №3 (37). – С.63–69.
6. Aguiar M., Andronis L., Pallan M., Högler W., Frew E. // European Journal of Clinical Nutrition. – 2019. https://doi.org/10.1038/s41430-019-0486-x
7. Aikaterini I. Trochoutsou, Vaia Kloukina, Konstantinos Samitas and Georgina Xanthou // Mini-Reviews in Medicinal Chemistry. – 2015. – Vol.15. – P.953–963.
8. Cashman K.D., Dowling K.G., Skrabakova Z., Gonzalez-Gross M., Valtuena J., De Henauw S., et al. // Am. J. Clin. Nutr. – 2016. – Vol.103, N4. – P.1033–1044.
9. Charoenngam N., et al. // Journal of Clinical Orthopaedics and Trauma. https://doi.org/10.1016/j.jcot.2019.07.004
10. Colotta F., Jansson B., Bonelli F. // J. Autoimmun. – 2017. – Vol.85. – P.78–97.
11. Eisman J.A., Bouillon R. // Bonekey Rep. – 2014. – Vol.3. – P.499–505.
12. Holick M.F., Binkley N.C., Bischoff-Ferrari H.A., Gordon C.M., Hanley D.A., Heaney R.P., Murad M.H., Weaver C.M. // J. Clin. Endocrinol. Metab. – 2011. – Vol.96, N7. – P.1911–1930.
13. Holick M.F., Chen T.C. // Am. J. Clin. Nutr. – 2008. – Vol.87, N4. – P.1080–1086.
14. Mukhtar M., Sheikh N., Suqaina S.K., et al. // Biomed. Res. Int. – 2019. doi:10.1155/2019/8326246
15. Pludowski P., Holick M.F., Pilz S., et al. // Autoimmun. Rev. – 2013. – Vol.12, N10. – P.976–989.
16. Pludowski P., et al. // J. Steroid. Biochem. Mol. Biol. – 2018 – Vol.175 – P.125–135.
17. Pludowski P., Grant W.B., Bhattoa H.P., et al. // International Journal of Endocrinology. – 2014 – doi:10.1155/2014/589587
18. Rudenka E., Rudenka A., Kastrytskaya O. // Standardy Medyczne. – 2015. – Vol.12, N5. – P.859–863.
19. Spiro A., Buttriss J.L. // Nutr. Bull. – 2014. – Vol.39. – P.322–350.
20. Yamamotoa E., Jørgensen Trine N. // Journal of Autoimmunity. – 2019. –Vol.100. – P.7–16.
Медицинские новости. – 2020. – №8. – С. 31-36.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.