Внимание! Статья адресована врачам-специалистам
Trisvetova E.L.
Belarusian State Medical University, Minsk
Diagnosis of interstitial lung diseases in systemic connective tissue diseases
Резюме. Интерстициальные заболевания легких, ассоциированные с системными заболеваниями соединительной ткани, нередко протекают без клинических проявлений. Прогрессирование поражения интерстиция легких обусловливает развитие дыхательной недостаточности, смертность от которой ухудшает прогноз жизни пациентов с системными заболеваниями соединительной ткани. Применение в начале установления диагноза аутоиммунного заболевания соединительной ткани и дальнейшее мониторирование результатов компьютерной томографии высокого разрешения, функционального исследования легких и диффузионной способности легких позволит выбрать эффективный метод лечения и прогнозировать течение заболевания.
Ключевые слова: интерстициальные заболевания легких, системные заболевания соединительной ткани, диагностика, инструментальные методы.
Медицинские новости. – 2021. – №7. – С. 22–28.
Summary. Interstitial lung diseases associated with systemic connective tissue diseases often occur without clinical manifestations. The progression of damage to the interstitium of the lungs leads to the development of respiratory failure, mortality from which worsens the prognosis of the life of patients with systemic diseases of the connective tissue. The use of connective tissue at the beginning of the diagnosis of an autoimmune disease and further monitoring of the results of high-resolution computed tomography, functional examination of the lungs and the diffusion capacity of the lungs will allow choosing an effective method of treatment and predicting the course of the disease.
Keywords: interstitial lung diseases, systemic connective tissue diseases, diagnostics, instrumental methods.
Meditsinskie novosti. – 2021. – N7. – P. 22–28.
Согласно сведениям Всемирной организации здравоохранения, известно более 300 нозологических форм интерстициальных, или диффузных, заболеваний легких (ИЗЛ), составляющих 20% всех болезней респираторной системы. Наиболее распространенные, идиопатический легочный фиброз и саркоидоз, обнаруживают в 50% случаев ИЗЛ, значительную долю составляют ИЗЛ с известными причинами, среди которых системные заболевания соединительной ткани. За истекшие годы отмечают рост распространенности заболеваний и медицинских затрат на их лечение. Вместе с тем диагностика ИЗЛ вызывает трудности, в 75–80% случаев допускают ошибки в распознавании болезни и поздно начинают лечение. Исследователи отмечают, что во многих случаях легочные изменения при ИЗЛ с известной этиологией являются причиной неблагоприятного течения заболеваний и прогноза.
Определение
ИЗЛ – это гетерогенная группа диффузных паренхиматозных болезней легких, при которых в патологический процесс (различные формы воспаления и фиброз) вовлекаются альвеолы и периальвеолярный интерстиций, что вызывает нарушения газообмена, вентиляционной функции легких по рестриктивному типу, диффузные интерстициальные изменения, выявляемые при рентгенологическом исследовании. Наряду с интерстицием при ИЗЛ в патологический процесс вовлекаются другие структуры респираторной системы: дыхательные пути, стенки кровеносных и лимфатических сосудов [1]. При различных ИЗЛ обнаруживают подобные клинические, рентгенологические и нередко гистологические изменения, обусловливающие сложности дифференциальной диагностики.
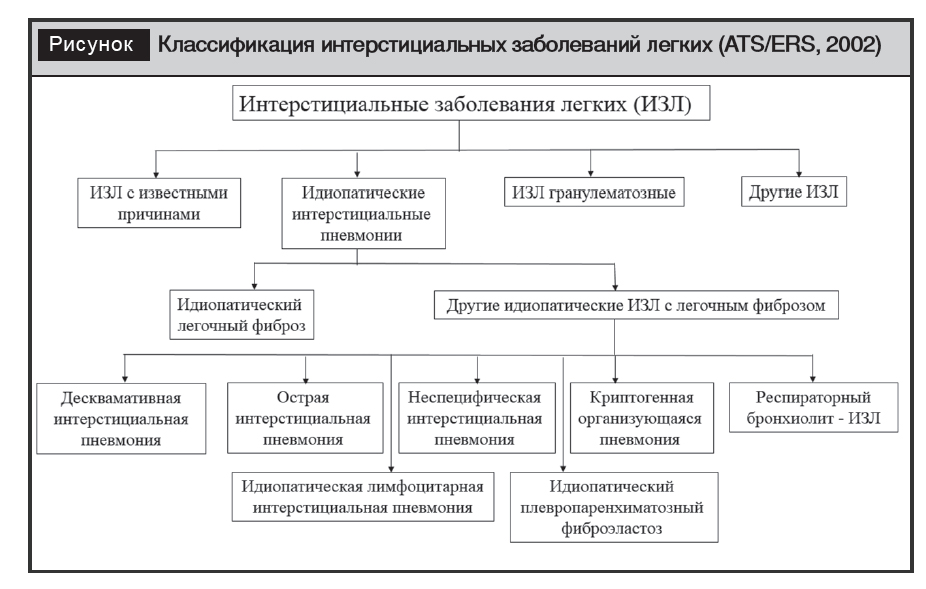
Классификация
Согласно классификации 2002 года, рассматривают 4 большие группы ИЗЛ (рисунок) [2]:
– ИЗЛ с известными причинами;
– идиопатические интерстициальные пневмонии (ИИП);
– гранулематозы;
– другие ИЗЛ.
Для клинико-рентгенологического и патологоанатомического сопоставления предложена классификация ИЗЛ с учетом течения заболевания, гистологических особенностей и связи с курением (табл. 1) [3].
Таблица 1. Течение, связь с курением, гистопатологические типы и клиническая классификация ИЗЛ
|
Группа идиопатических интерстициальных пневмоний
|
Клинико-рентгенологический и гистологический диагноз
|
Рентгенологические и морфологические признаки
|
|
Хронические фиброзирующие идиопатические интерстициальные пневмонии
|
Идиопатический легочный фиброз
Неспецифическая интерстициальная пневмония
|
Обычная интерстициальная пневмония
Неспецифическая интерстициальная пневмония
|
|
Идиопатические интерстициальные пневмонии, связанные с курением
|
Респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких
Десквамативная интерстициальная пневмония
|
Респираторный бронхиолит
Десквамативная интерстициальная пневмония
|
|
Острые/подострые идиопатические интерстициальные пневмонии
|
Криптогенная организующаяся пневмония
Острая интерстициальная пневмония
|
Организующаяся пневмония
Диффузное альвеолярное повреждение
|
Известные причины, вызывающие ИЗЛ, разнообразны, в эту группу включены системные заболевания соединительной ткани (системная красная волчанка, ревматоидный артрит, системный склероз, синдром Шегрена, смешанное заболевание соединительной ткани и др.), прием лекарственных препаратов (амфотерицин В, блеомицин, карбамазепин, метотрексат, флекаинид, циклофосфамид и др.), гиперчувствительный пневмонит, генетические заболевания (нейрофиброматоз, легочный альвеолярный протеиноз, болезнь Гоше, туберозный склероз и др.), профессиональные заболевания (асбестоз, беррилиоз, пневмокониоз, талькоз, легкое птичника, фермера, работников кофейной плантации и др.) [3].
Для системных заболеваний соединительной ткани, помимо ИЗЛ, характерными являются различные поражения респираторной системы, включающие бронхиолит, поражение плевры, бронхоэктазы, легочную гипертензию. В случае обнаружения ИЗЛ и аутоиммунных проявлений, не соответствующих критериям известных системных заболеваний соединительной ткани, диагностируют ИЗЛ с аутоиммунными признаками [3].
ИЗЛ выявляют у 40% пациентов с заболеваниями соединительной ткани преимущественно методом компьютерной томографии, поскольку клинические признаки неспецифичны: одышка, непродуктивный кашель, при исследовании функции внешнего дыхания – нормальные показатели или рестриктивные нарушения вентиляции (снижение общей емкости легких, нормальное соотношение объема форсированного выдоха за 1 секунду к форсированной жизненной емкости легких), снижение диффузионной способности легких по монооксиду углерода (DLCO), появление которых возможно не только за счет интерстициального поражения, но и за счет легочной гипертензии или эмфиземы [4].
ИЗЛ, ассоциированные с системными заболеваниями соединительной ткани, имеют лучший прогноз по сравнению с идиопатическими [4]. Признаки ИЗЛ обычно обнаруживают у пациентов, у которых диагностировано системное заболевание соединительной ткани, вместе с тем поражение легких изредка встречается как первое проявление аутоиммунного процесса [5].
Патологический процесс в легких при системных заболеваниях соединительной ткани обычно двусторонний, очаговый или распространенный, без четких границ, локализуется в нижних отделах легких и нередко сопровождается плевральным выпотом. Основные гистологические изменения при ИЗЛ и признаки, определенные по результатам компьютерной томографии, представлены в таблице 2 [6].
Таблица 2. Признаки ИЗЛ, выявляемые при гистологическом исследовании и компьютерной томографии при системных заболеваниях соединительной ткани
|
Гистопатологический паттерн
|
Характерные признаки при компьютерной томографии
|
|
Неспецифическая интерстициальная пневмония
|
Ретикулярная двусторонняя исчерченность, симптом «матового стекла», тракционные бронхоэктазы в нижних отделах легких
|
|
Обычная интерстициальная пневмония
|
Периферическое ретикулярно-узелковое снижение прозрачности легочной ткани базальных отделов с развитием «сотового легкого»
|
|
Диффузное альвеолярное повреждение
|
Симптом «матового стекла» с преобладанием в средних отделах, участки консолидации, утолщение меж- и внутридольковых перегородок
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
Симптом консолидации легочной ткани субплеврально, симптом «матового стекла», редко – диффузные узелковые сетчатые образования
|
|
Лимфоцитарная интерстициальная пневмония
|
Тонкостенные кисты, симптом «матового стекла», центродолевые узелки
|
|
Десквамативная интерстициальная пневмония
|
Мультифокальные или диффузные субплевральные изменения по типу «матового стекла» в нижних отделах легких, микрокисты, ретикулярная исчерченность
|
|
Диффузное альвеолярное повреждение
|
Симптом «матового стекла» с преобладанием в средних отделах, участки консолидации, утолщение меж- и внутридольковых перегородок
|
При ИЗЛ, ассоциированных с системными заболеваниями соединительной ткани, частота различных поражений легких неодинаковая (табл. 3).
Таблица 3. Частота ИЗЛ при системных заболеваниях соединительной ткани, выявляемых при гистологическом исследовании (из 7 с изменениями)
|
Заболевание, частота ИЗЛ
|
Гистопатологический паттерн
и частота среди определяемых ИЗЛ
|
|
Системный склероз, 45%
|
Неспецифическая интерстициальная пневмония – 80–90%
|
|
Обычная интерстициальная пневмония – 10–20%
|
|
Диффузное альвеолярное повреждение
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
|
Ревматоидный артрит, 5–58%
|
Обычная интерстициальная пневмония – 50–60%
|
|
Неспецифическая интерстициальная пневмония – 30–60%
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
|
Лимфоцитарная интерстициальная пневмония
|
|
Диффузное альвеолярное повреждение
|
|
Десквамативная интерстициальная пневмония
|
|
Полимиозит/дерматомиозит, 30–70%
|
Неспецифическая интерстициальная пневмония
|
|
Обычная интерстициальная пневмония
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
|
Диффузное альвеолярное повреждение
|
|
Синдром Шегрена, до 25%
|
Неспецифическая интерстициальная пневмония
|
|
Лимфоцитарная интерстициальная пневмония
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
|
Обычная интерстициальная пневмония
|
|
СКВ, 2–8%
|
Острая интерстициальная пневмония
|
|
Неспецифическая интерстициальная пневмония
|
|
Десквамативная интерстициальная пневмония
|
|
Обычная интерстициальная пневмония
|
|
Лимфоцитарная интерстициальная пневмония
|
|
Смешанное заболевание
соединительной ткани, 20–60%
|
Неспецифическая интерстициальная пневмония
|
|
Облитерирующий бронхиолит с организующейся пневмонией
|
|
Обычная интерстициальная пневмония
|
|
Диффузное альвеолярное повреждение
|
Для диагностики ИЗЛ, ассоциированных с системными заболеваниями соединительной ткани, важным является исследование, направленное на обнаружение основного аутоиммунного заболевания, включающее результаты физикальных, инструментальных, лабораторных, иммунологических методов. В случаях трудности идентификации поражения легких выполняют биопсию ткани с последующим гистологическим исследованием.
Системная красная волчанка (СКВ)
В патологический процесс при СКВ вовлекаются все компоненты дыхательной системы: верхние дыхательные пути, паренхима легких, плевра, сосуды, дыхательные мышцы. К первичным проявлениям СКВ относятся острая интерстициальная пневмония (острый волчаночный пневмонит), неспецифическая интерстициальная пневмония, легочные (альвеолярные) геморрагии, легочная гипертензия, тромбоэмболическое поражение легочных артерий, легочный васкулит [6].
Острый волчаночный пневмонит развивается остро или подостро, начало заболевания – с лихорадки, сухого кашля, изредка кровохарканья, быстро прогрессирующей одышки. Рентгенологические признаки неспецифичны: инфильтративные изменения одно- или двусторонние, преимущественно в нижних отделах легких. При гистологическом исследовании выявляют повреждения и некроз альвеолярно-капиллярной мембраны, инфильтрацию клетками воспаления, отек, геморрагии, микроангиит с фибриновыми тромбами и нейтрофильной инфильтрацией [5]. Возможно развитие диффузного альвеолярного кровоизлияния как проявление СКВ или антифосфолипидного синдрома [6]. Острый волчаночный пневмонит встречается в 1–4% случаев, смертность в результате развития пневмофиброза и прогрессирующей дыхательной недостаточности составляет 50% [7].
Неспецифическая интерстициальная пневмония встречается часто по сравнению с острым волчаночным пневмонитом, протекает мало- или бессимптомно, приводя постепенно к фиброзу интерстиция и дыхательной недостаточности. В клинической картине отмечают кашель с незначительным отделением мокроты, постепенно нарастающую одышку, плевральные боли. При аускультации выслушивают крепитацию (феномен «Велькро» или «целлофановые» хрипы) над нижними отделами обоих легких. При спирографии – снижение показателей функции внешнего дыхания, указывающих на рестриктивные нарушения, снижение диффузионной способности легких – у 80% пациентов, опережающие появление рентгенологических проявлений. При рентгенологическом исследовании неспецифическую интерстициальную пневмонию диагностируют в 3–5% случаев, при выполнении компьютерной томографии – в 30–40% [8].
Редко (0,5–1,1%), преимущественно у женщин (Ж:М=17:1), длительно болеющих СКВ, обнаруживают синдром сморщенного легкого (shrinking lung syndrome), характеризующийся прогрессирующей одышкой, болью в грудной клетке, обусловленной вовлечением плевры, плевритом (в 60% случаев), высоким стоянием куполов диафрагмы и уменьшением объема легких без паренхиматозных изменений [9]. Диагностируют синдром сморщенного легкого, исключив другие поражения респираторной системы при СКВ, на основании результатов клинического и инструментальных (функция внешнего дыхания, исследование диффузионной способности легких, компьютерная томография высокого разрешения) исследований.
Согласно наблюдениям, при СКВ изредка встречаются десквамативная и лимфоцитарная интерстициальная пневмонии. Гистологические изменения характеризуются периваскулярной инфильтрацией, перибронхиальной лимфоидной гиперплазией и интерстициальным фиброзом [7].
Умеренный или выраженный фиброз с тяжелой дыхательной недостаточностью редко развивается при СКВ [10].
Системный склероз
Одной из характерных висцеральных локализаций склеродермического процесса являются легкие. Поражение легких включает все гистологические варианты интерстициальных пневмоний: обычную интерстициальную пневмонию, неспецифическую интерстициальную пневмонию, облитерирующий бронхио-лит с организующейся пневмонией, лимфоцитарную интерстициальную пневмонию, диффузные альвеолярные геморрагии [11]. Наиболее частым гистологическим вариантом является неспецифическая интерстициальная пневмония (80–90%).
При морфологическом исследовании определяют признаки воспаления с картиной альвеолита и фиброза разной степени выраженности, утолщение альвеолярных стенок, интимы прекапиллярных артериол с сужением и полной облитерацией просвета сосуда. Прогрессирующий пневмосклероз, фиброзирующий альвеолит, легочную гипертензию выявляют при подостром и остром течении системного склероза. Нередко в биоптатах одной доли легкого обнаруживают признаки острой интерстициальной и неспецифической интерстициальной пневмонии, в связи с этим трудно дифференцировать преобладание того или другого патологического процесса [12].
Описывают две морфологические формы интерстициального поражения легких при системном склерозе: компактный пневмосклероз с диффузным разрастанием соединительной ткани и образованием очагов склероза и гиалиноза, кистовидный пневмосклероз, который часто сопровождается образованием полостей, расположенных субплеврально [13].
Клинические признаки отсутствуют или неспецифичны: непродуктивный кашель и одышка, при выслушивании над легкими – стойкая крепитация над базальными отделами. При исследовании функции внешнего дыхания обнаруживают рестриктивные нарушения [12].
При мультиспиральной компьютерной томографии поражение легких выявляют в 80% случаев, при этом фиброзирующий процесс в интерстиции впервые выявляют на 4–6-м году болезни [14]. Изменения в легких, как правило, двусторонние ретикулярные с локализацией в нижних отделах легких, характерным является симптом «матового стекла» и ячеистый рисунок («сотовое» легкое) [15]. Фиброзные плевральные наложения обнаруживают у большинства пациентов.
Изменения функции внешнего дыхания и DLCOпроисходят рано, в течение первых трех лет болезни пациентов, независимо от наличия или отсутствия других симптомов поражения легких. При динамическом наблюдении снижение показателей на 10–15% от исходного уровня свидетельствует о прогрессировании процесса в легких [15].
К факторам риска развития или прогрессирования ИЗЛ у пациентов с системным склерозом и ИЗЛ относятся афроамериканская этническая принадлежность, исходная форсированная жизненная емкость легких <70%, выраженный фиброз легких по результатам рентгенологического исследования, диффузная форма системного склероза, мужской пол, пожилой возраст в начале заболевания, позитивность по антителам к Scl-70, высокий кожный счет [16].
Частота поражения легких при системном склерозе составляет 30–90%, в том числе интерстициальное поражение, легочная гипертензия и пневмонии – 50%. В отличие от других идиопатических интерстициальных пневмоний при системном склерозе интерстициальное поражение легких часто протекает волнообразно, с медленным прогрессированием и периодами стабилизации процесса [12].
Тяжелое прогрессирующее поражение легких развивается редко, в 10–15% случаев, тем не менее до 60% смертности пациентов с системным склерозом связывают с ИЗЛ [11, 17]. Смертность лиц с системным склерозом и ИЗЛ в три раза выше по сравнению с пациентами с системным склерозом без ИЗЛ [17].
Ревматоидный артрит
При ревматоидном артрите первичные легочные проявления представлены заболеваниями плевры, верхних и нижних дыхательных путей (артрит перстнечерпаловидного сустава, бронхоэктазы, фолликулярный или облитерирующий бронхиолит, диффузный панбронхиолит), острой эозинофильной пневмонией, диффузным повреждением альвеол, апикальным фибробуллезным заболеванием (апикальная эмфизема и базальный пневмофиброз), амилоидозом, ревматоидными узлами, сосудистыми заболеваниями легких (легочная гипертензия, васкулит, диффузные альвеолярные геморрагии с капилляритами) [18].
Поражение интерстиция легких относится к основным легочным проявлениям у пациентов с ревматоидным артритом, протекает часто в виде обычной интерстициальной пневмонии, характеризующейся плохим прогнозом, неспецифической интерстициальной пневмонии с более благоприятным течением, облитерирующего бронхиолита с организующейся пневмонией или лимфоцитарной пневмонии [19]. В большинстве случаев ИЗЛ обнаруживают у пациентов (чаще у мужчин) 50–60 лет, курильщиков, при наличии клинических признаков ревматоидного артрита, изредка поражение легких предшествует развернутой клинической картине заболевания.
При рентгенологическом исследовании у пациентов с ревматоидным артритом выявлены четыре паттерна: острая интерстициальная пневмония с двусторонними ретикулярными субплевральными изменениями с ячеистым рисунком или без него; неспецифическая интерстициальная пневмония с преобладанием симптома «матового стекла»; воспалительные изменения с центрилобулярными ретикулярными изменениями с расширением бронхов; облитерирующий бронхиолит с организующейся пневмонией с участками консолидации [20, 21].
В клинической практике у пациентов с ревматоидным артритом в большинстве случаев встречается острая интерстициальная пневмония (56%), реже выявляют неспецифическую интерстициальную пневмонию (33%), изредка – организующуюся (11%) и лимфоцитарную пневмонии [21].
При продолжительности ревматоид-ного артрита более 2 лет у 58% лиц обнаруживают ИЗЛ по результатам исследований методом компьютерной томографии высокого разрешения, сцинтиграфии с технецием 99-м, тестирования функции легких (рестриктивные нарушения функции внешнего дыхания и снижение DLCO) и бронхоальвеолярной лаважной жидкости (преобладание нейтрофилов и макрофагов). В 76% случаев у пациентов с инструментально выявленными ИЗЛ поражение легких протекало скрыто, отсутствовали клинические признаки [22].
ИЗЛ у больных ревматоидным артритом являются одной из наиболее значимых причин смертности: при ревматоидном артрите с ИЗЛ смертность на 6–13% выше по сравнению с популяционной. Прогноз жизни таких пациентов ухудшается при прогрессировании ИЗЛ с развитием дыхательной недостаточности, на смертность при ИЗЛ приходится до 20% случаев смерти лиц с ревматоидным артритом [23].
Полимиозит/дерматомиозит
Среди легочной патологии при полимиозите/дерматомиозите встречаются поражения интерстиция, сосудов малого круга кровообращения, аспирационные и бактериальные пневмонии. Частота аспирационных и бактериальных пневмоний составляет 17%, ИЗЛ – 65%, встречаются лекарственно-индуцированное поражение легких, легочная гипертензия, диффузные альвеолярные геморрагии и осложнения в виде пневмомедиастинума, пневмоторакса. Непаренхиматозную дыхательную недостаточность обнаруживают в 5% случаев при поражении диафрагмы и межреберных мышц [24].
ИЗЛ относятся к наиболее распространенным заболеваниям респираторной системы (19,9–78%), они влияют на прогноз жизни и выбор более агрессивных методов лечения заболевания [24]. К основным гистологическим паттернам ИЗЛ, ассоциированным с полимиозитом/дерматомиозитом, относятся следующие: неспецифическая интерстициальная пневмония, обычная интерстициальная пневмония, облитерирующий бронхиолит с организующейся пневмонией, диффузное альвеолярное повреждение, лимфоцитарная пневмония [25].
Поражение легких, ассоциированное с полимиозитом/дерматомиозитом, нередко протекает мало- или бессимптомно, с незначительными рентгенологическими признаками в виде базальных ретикулярных изменений. В других случаях диагностируют ИЗЛ с хроническим или острым быстропрогрессирующим течением, приводящим к пневмофиброзу и выраженной дыхательной недостаточности. Клинические признаки – одышка и кашель – изредка предшествуют кожным и мышечным симптомам, в большинстве случаев развиваются одновременно с симптомами поражения мышц и кожи.
Частым вариантом при рентгенологическом исследовании органов грудной клетки является неспецифическая интерстициальная пневмония с ретикулярными изменениями и/или нарушениями по типу «матового стекла» с/без зон консолидации. Этот вариант ИЗЛ является более благоприятным для лечения по сравнению с остальными [26]. При появлении «сотового» легкого, свидетельствующего о развитии фиброза легких, отмечают незначительный эффект от терапии.
Исследование функции внешнего дыхания проводят для определения степени выраженности рестриктивных нарушений (снижение общей емкости легких, форсированной жизненной емкости легких, а также DLCO) и степени дыхательной недостаточности, при прогрессировании которой ухудшается прогноз жизни пациента с полимиозитом/дерматомиозитом [25].
В случае типичной клинической картины ИЗЛ, ассоциированных с полимиозитом/дерматомиозитом, отсутствует необходимость в выполнении биопсии легкого и морфологическом подтверждении поражения легких.
Известно, что одним из основных маркеров ИЗЛ, ассоциированных с полимиозитом/дерматомиозитом, является позитивность по антисинтетазным телам, среди которых отмечают анти-Jo1. При наличии Jо1-антител у пациентов в 90% случаев обнаруживают ИЗЛ, при этом отмечают рефрактерность к лечению и высокую смертность от дыхательной недостаточности [27]. Исследователи отмечают, что в целом антисинтетазный синдром, наиболее тяжелый подтип полимиозита/дерматомиозита, у пациентов, положительных по другим типам антисинтетазных антител, протекает с поражением легких в трех формах: первая – быстро прогрессирующий легочный фиброз (синдром Хаммена – Рича), с нарастающей одышкой, лихорадкой и непродуктивным кашлем; для второй формы характерна постепенно нарастающая одышка, предшествующая поражению мышц; при третьей форме клинические признаки ИЗЛ отсутствуют, изменения обнаруживают при компьютерной томографии высокого разрешения и функциональном исследовании легких [26].
К предикторам неблагоприятного течения ИЗЛ, ассоциированного с полимиозитом/дерматомиозитом, относятся следующие: наличие anti-Jo1-антител; суставнои? синдром; амиопатическии? вариант течения болезни; начало заболевания в пожилом возрасте; микроангиопатия и дигитальные инфаркты; наличие острого фиброзирующего альвеолита (по типу синдрома Хаммена – Рича) в дебюте заболевания; снижение форсированной жизненной емкости легких менее чем на 60–45% в начальный период болезни; наличие anti-Ro/SSA-аутоантител в сыворотке крови; неи?трофильныи? альвеолит по результатам исследования бронхоальвеолярного лаважа; гистологическая картина обычной интерстициальной пневмонии [27].
Смертность при ИЗЛ, ассоциированных с полимиозитом/дерматомиозитом, в результате прогрессирующей дыхательной недостаточности достигает 40% [25].
Синдром Шегрена
Поражение респираторной системы при синдроме Шегрена встречается в виде изменений дыхательных путей (фолликулярный бронхит и бронхио-лит) с обструктивным синдромом, сухостью слизистой оболочки трахео-бронхиального дерева и ИЗЛ. ИЗЛ обнаруживают в 9–22% случаев, наиболее типичным является развитие прогрессирующей неспецифической интерстициальной пневмонии (45%), реже – обычной интерстициальной пневмонии (16%), лимфоцитарной интерстициальной пневмонии (15%) и облитерирующего бронхиолита с организующейся пневмонией (11%) [28]. У 10–51% пациентов признаки ИЗЛ появляются задолго до развития признаков синдрома Шегрена [29].
Клинические симптомы, как правило, представлены непродуктивным кашлем и одышкой, крепитацией в заднебазальных отделах легких при аускультации, при тестировании функции легких обнаруживают рестриктивные нарушения и снижение диффузионной способности легких к окиси углерода. Обычное рентгенологическое исследование не всегда информативно, для диагностики поражения легких необходимо выполнить компьютерную томографию, при которой выявляют линейные ретикулярные тяжи, симптом «матового стекла», утолщение междольковых перегородок, кисты, фиброз. Наличие воздушных кист – характерный признак при синдроме Шегрена, редко определяемый при других системных заболеваниях соединительной ткани [30].
На компьютерных томограммах при неспецифической интерстициальной пневмонии у пациентов с синдромом Шегрена обнаруживают симметричные базальные ретикулярные изменения, тракционные бронхоэктазы, перибронховаскулярные расширения, участки субплевральных уплотнений. Исходы неспецифической интерстициальной пневмонии различные: медленное прогрессирование, стабильное с незначительными нарушениями функции легких, прогрессирующее с необратимыми изменениями, несмотря на проводимое лечение [31].
Обычную интерстициальную пневмонию диагностируют при компьютерной томографии в виде двусторонних ретикулярных изменений с тракционными бронхоэктазами и небольшими кистозными образованиями. К особенностям рентгенологической картины относится неоднородность интерстициального фиброза, чередующегося с участками нормальной паренхимы, расположенного преимущественно субплеврально и по периферии долек. При гистологическом исследовании выявляют рассеянные очаги фибробластов, минимальные проявления интерстициального воспаления. Прогноз обычной интерстициальной пневмонии, ассоциированной с синдромом Шегрена, неблагоприятный, поскольку быстро появляются признаки и прогрессирование дыхательной недостаточности [32].
Лимфоцитарная интерстициальная пневмония при синдроме Шегрена встречается чаще по сравнению с другими системным заболеваниями соединительной ткани. Клинические признаки также неспецифичны (кашель, одышка), при аускультации – над нижними отделами легких крепитация, при исследовании вентиляционной функции легких обнаруживают рестриктивные нарушения.
При компьютерной томографии легких выявляют утолщение бронхо-васкулярных пучков, узелки и симптом «матового стекла». Результаты гистологических исследований свидетельствуют о диффузной пролиферации поликлональных лимфоцитов и плазматических клеток в легочной паренхиме с лимфоидными фолликулами и зародышевыми центрами [33].
К факторам риска развития ИЗЛ, ассоциированных с синдромом Шегрена, относят пожилой возраст, курение, гипергаммаглобулинемию, повышенный титр ревматоидного фактора, или титры антиядерных антител, позитивность по анти-SSA или SSB-антител, повышенный уровень С-реактивного белка и сниженный уровень С3 в сыворотке крови [34].
Смешанное заболевание соединительной ткани
ИЗЛ при смешанном заболевании соединительной ткани не проявляются и не распознаются в начале болезни, их диагностируют по результатам компьютерной томографии легких в 48% случаев. Исследователи отмечают, что у большинства пациентов поражение легких клинически протекает малосимп-томно и выявление ИЗЛ возможно лишь при инструментальном исследовании. К основным диагностическим методам изучения поражения легких относятся исследование функции внешнего дыхания (рестриктивные нарушения), DLCO (снижение диффузионной способности легких к монооксиду углерода), компьютерная томография легких высокого разрешения и сцинтиграфия с 99mTc [35].
Поскольку смешанное заболевание соединительной ткани имеет клинические признаки СКВ, системного склероза, полимиозита/дерматомиозита, могут возникать ИЗЛ, характерные для любых из перечисленных системных заболеваний соединительной ткани. Наиболее распространенное ИЗЛ при смешанном заболевании соединительной ткани – неспецифическая интерстициальная пневмония, характеризующаяся в большинстве случаев негрубыми ретикулярными изменениями, симптомом «матового стекла» и утолщением межальвеолярных перегородок в нижних отделах легких. Результаты компьютерной томографии напоминают изменения, выявляемые при системном склерозе [36, 37].
В целом при смешанном заболевании соединительной ткани ИЗЛ протекают с более благоприятным прогнозом по сравнению с другими системными заболеваниями соединительной ткани. У пациентов с распространенным фиброзом легких, часто старшего возраста, с выраженными вентиляционными нарушениями отмечают высокую смертность от дыхательной недостаточности [35].
Заключение
ИЗЛ относятся к частым проявлениям системных заболеваний соединительной ткани и в большинстве случаев при прогрессирующем течении неблагоприятно влияют на прогноз жизни. В связи с тем, что патологические механизмы формирования ИЗЛ, ассоциированных с системными заболеваниями соединительной ткани, определены не полностью, прогнозирование поражения легких сомнительно. Как правило, ИЗЛ в начале развития заболевания протекают мало- или бессимптомно, вызывая непродуктивный кашель и одышку и обусловливая скудные физикальные данные при перкуссии и аускультации грудной клетки. В диагностике ИЗЛ, ассоциированных с системными заболеваниями соединительной ткани, на ранних этапах выявления аутоиммунного заболевания наиболее информативными считают результаты инструментальных методов исследования респираторной системы: рентгенографии органов грудной клетки, компьютерной томографии высокого разрешения, функции внешнего дыхания и диффузионной способности легких, сцинтиграфии легких. Мониторирование качественных и количественных характеристик легких при компьютерной томографии высокого разрешения влияет на выбор медикаментозной тактики пациента, а функциональных показателей – на степень дыхательной недостаточности, определяющей прогноз жизни. В дифференциальной диагностике с ИЗЛ, ассоциированных с системными заболеваниями соединительной ткани, с идиопатическими ИЗЛ и легочным фиброзом необходимо выявлять диагностические критерии аутоиммунного заболевания, в редких случаях применять биопсию легкого и морфологическое подтверждение диагноза.
ЛИТЕРАТУ РА
1. American Thoracic Society/European Respiratory Society International Multidisciplinary Consensus Classification of the Idiopathic Interstitial Pneumonias // J. Respir. Crit. Care Med. – 2002. – Vol.165, N2. – P.277–304.
2. Kadoch M.A., Cham M.D., Beasley M.., Ward T.J., Jacoi A.H., Eber C.D., Padilla M.L. Idiopathic interstitial pneumonias: a radiology-pathology correlation based on the revised 2013 American Thoracic Society-European Respiratory Society classification system // Curr. Probl. Diagn. Radiol. – 2015. – Vol.44, N1. – P.15–25.
3. Cottin V., Hirani N.A., Hotchkin D.L., Nambiar A.M., Ogura T., Otaola M., Skowasch D., Park J.S., Poonyagariyagorn H.K., Wuyts W., Wells A.U. Presentation, diagnosis and clinical course of the spectrum of progressive-fibrosing interstitial lung diseases // Eur. Respir. Rev. – 2018. – N27 (150). – P.180076.
4. Montesi S., Fisher J.H., Martinez F.J., Selman M., Pardo A., Johannson K.A. Update in Interstitial Lung Disease // Am. J. Respir. Critical. Care Med. – 2019. – Vol.202, N4. – P.500–507.
5. Vij R., Strek M.E. Diagnosis and Treatment of Connective Tissue Disease-Associated Interstitial Lung Disease //Chest. – 2013. – Vol.143, N3. – P.814–824.
6. Fischer A., Antoniou K.M., Brown K.K., Cadranel J., Corte T.J., du Bois R.M., Lee J.S., Leslie K.O., Lynch D.A., Matteson E.L., Mosca M., Noth I., Richeldi L., Strek M.E., Swigris J.J., Wells A.U., West S.G., Harold R., Collard H.R., Cottin V. on behalf of the “ERS/ATS Task Force on Undifferentiated Forms of CTD-ILD”. An official European Respiratory Society/American Thoracic Society research statement: interstitial pneumonia with autoimmune features // Eur. Respir. J. – 2015. – Vol.46, N4. – P.976–987.
7. Mira-Avendano I., Abril A., Burger C.D., Dellaripa P.F., Fischer A., Gotway M.B., Lee A.S., Lee J.S., Matteson E.L., Yi E.S., Ryu J.H. Interstitial Lung Disease and Other Pulmonary Manifestations in Connective Tissue Diseases // Mayo Clin. Proc. – 2019. – Vol.94, N2. – P.309–325.
8. Oliveira R.P., Ribeiro R., Melo L., Grima B., Oliveira S., Alves J.D. Connective tissue disease-associated interstitial lung disease // Pulmonol. – 2020. – S2531–0437(20)30004-0.
9. Borelli H., Narvaez J., Alegre J.J., Castellvi I., Mitjavila F., Aparicio M., Armengol E., Molina-Molina M., Nolla J.M. Shrinking lung syndrome in systemic lupus erythematosus. A case series and review of the literature // Medicine (Baltimore). – 2016. – Vol.95, N33. – e4626.
10. Fischer A., Strek M., Cottin V., Dellaripa P.E., Bernstein E.J., Brown K.K., Danoff S.K., Distler O., Hirani N., Jones K.D., Khanna D., Lee J.S., Lynch D.A., Maher T.M., Millar A.B., Raghu G., Silver R.M., Steen V.D., Volkmann E.R., Mullan R.H., O’Dwyer D.N., Donnelly S.C. Proceedings of the American College of Rheumatology/Association of Physicians of Great Britain and Ireland Connective Tissue Disease-Associated Interstitial Lung Disease Summit: A Multidisciplinary Approach to Address Challenges and Opportunities // Arthritis Rheumatol. – 2019. – Vol.71, N2. – P.182–195.
11. Steen V., Medsger T. Changes in causes of death in systemic sclerosis, 1972–2002 // Ann. Rheum. Dis. – 2007. – Vol.66, N7. – P.940–944.
12. Cottin V., Brown K. Interstitial lung disease associated with systemic sclerosis (SSc-ILD) // Respir. Res. – 2019. – Vol.20, N13.
13. Fischer A., Swigris J.J., Groshong S.D., Cool C.D., Sachin H., Lynch D.A., Curran-Everett D., Gillis J.A., Meechan R.T., Brown K.K. Clinically significant interstitial lung disease in limited scleroderma: histopathology, clinical features, and survival // Chest. – 2008. – Vol.134, N3. – P.601–605.
14. Fischer A., Patel N.M., Volkmann E.R. Interstitial Lung Disease in Systemic Sclerosis: Focus on Early Detection and Intervention // Rheumatol. – 2019. – N11. – P.283–307.
15. Showalter K., Hoffmann A., Rouleau G., Aaby D., Lee J., Richardson C., Dematte J., Agrawal R., Chang R.W., Hinchcliff M. Performance of Forced Vital Capacity and Lung Diffusion Cutpoints for Associated Radiographic Interstitial Lung Disease in Systemic Sclerosis // J. Rheumatol. – 2018. – Vol.45, N11. – P.1572–1576.
16. Jaeger V.K., Wirz E.G., Allanore Y., Rossbach P., Riemekasten G., Hachulla E., Distler O., Airo P., Carreira P.E., Gurman A.B., Tikly M., Vettori S., Damjanov N., et al. EUROSTAR. Incidences and Risk Factors of Organ Manifestations in the Early Course of Systemic Sclerosis: A Longitudinal EUSTAR Study // PLoS One. – 2016. – Vol.11, N10. – e0163894.
17. Rubio-Rivas M., Royo C., Simeon C.P., Corbella X., Fonollosa V. Mortality and survival in systemic sclerosis: systematic review and meta-analysis // Semin Arthritis Rheum. – 2014. – Vol.44, N2. – P.208–219.
18. Kim E.J., Collard H.R., King T.E. Rheumatoid Arthritis-Associated Interstitial Lung Disease. The Relevance of Histopathologic and Radiographic Pattern // Chest. – 2009. – Vol.136, N5. – P.1397–1405.
19. Olson A.L., Swigris J.J., Sprunger D.B., Fischer A., Fernandez-Perez E.R., Solomon J., Murphy J., Cochen M., Raghu G., Brown K.K. Rheumatoid Arthritis-Interstitial Lung Disease-associated Mortality // Am. J. Respir. Crit. Care Med. – 2011. – Vol.183, N3. – P.372–378.
20. Afeltra A., Zennaro D., Garzia P., Gigante A., Vadacca M., Ruggiero A., Dardes N., Navajas M.F., Zobel B.B., Amoroso A. Prevalence of interstitial lung involvement in patients with connective tissue diseases assessed with high-resolution computed tomography // Scand. J. Rheumatol. – 2006. – Vol.35, N5. – P.388–394.
21. Tanaka N., Kim J.S., Newell J.D., Brown K.K., Cool C.D., Meechan R., Emoto T., Matsumoto T., Lynch D. Rheumatoid arthritis-related lung diseases: CT findings // Radiology. – 2004. – Vol.232, N1. – P.81–91.
22. Gabbay E., Tarala R., Will R., Adler B., Cameron D., Lake F.R. Interstitial lung disease in recent onset rheumatoid arthritis // Am. J. Respir. Crit. Care Med. – 1997. – Vol.156 (Pt 1). – P.528–535.
23. Ascherman D.P. Interstitial lung disease in rheumatoid arthritis // Curr. Rheumatol. Rep. – 2010. – Vol.12, N5. – P.363–369.
24. Kalluri M., Oddis C.V. Pulmonary Manifestations of the Idiopathic Inflammatory Myopathies // Clin. Chest. Med. – 2010. – Vol.31. – P.501–512.
25. Zhang L., Wu G., Gao D., Liu G., Pan L., Ni L., Li Z., Wang Q. Factors Associated with Interstitial Lung Disease in Patients with Polymyositis and Dermatomyositis: A Systematic Review and Meta-Analysis // PLoS One. – 2016. – Vol.11, N5. – e0155381.
26. Marie I., Hatron P.Y., Dominique S., Cherin P., Mouthon L., Menard J.-F. Short-term and long-term outcomes of interstitial lung disease in polymyositis and dermatomyositis: a series of 107 patients // Arthritis Rheum. – 2011. – Vol.63, N11. – P.3439–3447.
27. Hallowell R.W., Ascherman D.P., Danoff S.K. Pulmonary manifestations of polymyositis/dermatomyositis // Semin. Respir. Crit. Care Med. – 2014. – Vol.35, N2. – P.239–248.
28. Palm O., Garen T., Enger T.B., Jensen J.L., Lund M-B., Aalokken T.M., Gran J.T. Clinical pulmonary involvement in primary Sjogren’s syndrome: prevalence, quality of life and mortality – a retrospective study based on registry data // Rheumatol. (Oxford). – 2013. – Vol.52, N1. – P.173–179.
29. Flament T., Bigot A., Chaigne B., Henique H., Diot E., Marchand-Adam S. Pulmonary manifestations of Sjogren’s syndrome // Eur. Respir. Rev. – 2016. – N25 (140). – P.110–123.
30. Daniels T.E., Cox D., Shiboski C.H., Schiodt M., Wu A., Lanfranchi H., Umehara H., Yan Zhao Y., Stephen Challacombe S., Mi Y Lam M.Y., De Souza Y., Schiodt J., Holm H., Patricia A.M., Bisio P.A.M., Gandolffo M.S., Sawaki T., Li M., Zhang W., Vargese-Jacob B., Ibsen P., Keszler A., Kurose N., Nojima T., Odell E., Criswell L.A., Jordan R., Greenspan J.S. Associations between salivary gland histopathologic diagnoses and phenotypic features of sjogren’s syndrome among 1,726 registry participants // Arthritis Rheum. – 2011. – Vol.63, N7. – P.2021–2030.
31. Roca F., Dominique S., Schmidt J., Smail A., Duchaut P., Levesque H., Marie I. Interstitial lung disease in primary Sjögren’s syndrome // Autoimmun. Rev. – 2017. – Vol.16, N1. – P.48–54.
32. Manfredi A., Sebstiani M., Cerri S., Cassone G., Bellini P., Casa G.D., Luppi F., Ferri C. Prevalence and characterization of non-sicca onset primary Sjögren syndrome with interstitial lung involvement // Clin. Rheumatol. – 2017. – Vol.36, N6. – P.1261–1268.
33. Luppi F., Sebastiani M., Silva M., Sverzellati N., Cavazza A., Salvarani C., Manfredi A. Interstitial lung disease in Sjögren’s syndrome: a clinical review // Clin. Exp. Rheumatol. – 2020. – Vol.38, Suppl.126 (4). – P.291–300.
34. Sogkas G., Hirsch S., Olsson K.M., Hinrichs J., Thiele T., Seeliger T., Skripuletz T., Schmidt R.E., Witte T., Jablonka A., Ernst D. Lung Involvement in Primary Sjögren’s Syndrome – An Under-Diagnosed Entity // Front Med. (Rheumatol.). – 2020. – N7. – P.332.
35. Bodolay E., Szekanecz Z., Devenyi K., Galuska L., Csipo I., Vegh J., Szegedi G. Evaluation of interstitial lung disease in mixed connective tissue disease (MCTD) // Rheumatol. Oxford. – 2005. – Vol.44, N5. – P.656–661.
36. Prakash U.B. Respiratory complications in mixed connective tissue disease // Clin. Chest. Med. – 1998. – Vol.19, N4. – P.733–746.
37. Hajas A., Szodoray P., Nakken B., Gaal J., Zöld E., Laczik R., Demeter N., Nagy G., Szekanecz Z., Zecher M., Szegedi G., Bodolay E. Clinical course, prognosis, and causes of death in mixed connective tissue disease // J. Rheumatol. – 2013. – Vol.40, N7. – P.1134–1142.
Медицинские новости. – 2021. – №7. – С. 22-28.
Внимание! Статья адресована врачам-специалистам. Перепечатка данной статьи или её фрагментов в Интернете без гиперссылки на первоисточник рассматривается как нарушение авторских прав.